
分析 (1)某溶液常温下刚析出Mg(OH)2固体时,达到Mg(OH)2的溶解平衡,即有:c(Mg2+)•c(OH-)2=Ksp[Mg(OH)2]=5×10-12,据此解答;
(2)CH3COONH4溶液为中性,说明醋酸和一水合氨电离程度相等,且CH3COOH溶液加到NaHCO3溶液中有气体放出,说明CH3COOH大于H2CO3,则一水合氨电离程度大于H2CO3电离程度,根据铵根离子水解程度和HCO3-水解程度相对大小判断NH4HCO3溶液的pH;
(3)碱能抑制水的电离,而在碱溶液中,氢氧根几乎全部来自于碱的电离,而氢离子来自于水的电离;
(4)在能水解的正盐溶液中,盐类的水解对水的电离有促进作用,且氢离子和氢氧根全部来自于水的电离,据此分析.
解答 解:(1)已知常温下,Ksp[Mg(OH)2]=5×10-12,某溶液常温下刚析出Mg(OH)2固体时,即达到Mg(OH)2的溶解平衡,即有:c(Mg2+)•c(OH-)2=Ksp[Mg(OH)2]=5×10-12,而c(Mg2+)=5×10-2mol/L,故有:5×10-2mol/L×c(OH-)2=Ksp[Mg(OH)2]=5×10-12,解得c(OH-)=10-5mol/L,则有:c(H+)=10-9mol/L,则溶液的pH=-lgc(H+)=9.故答案为:9;
(2)CH3COONH4溶液为中性,说明醋酸和一水合氨电离程度相等,且CH3COOH溶液加到NaHCO3溶液中有气体放出,说明CH3COOH大于H2CO3,则一水合氨电离程度大于H2CO3电离程度,所以水解程度:HCO3->NH4+,所以NH4HCO3溶液的pH>7,故答案为:>;
(3)碱能抑制水的电离,而在碱溶液中,氢氧根几乎全部来自于碱的电离,而氢离子来自于水的电离,故在pH=11的KOH溶液中,氢离子浓度c(H+)=10-11mol/L,全部来自于水,而由水电离出的氢离子和水电离出的氢氧根的浓度相同,故此溶液中水电离出的氢氧根的浓度c(OH-)=c(H+)=10-11mol/L;故答案为:10-11;
(4)在能水解的正盐溶液中,盐类的水解对水的电离有促进作用,且氢离子和氢氧根全部来自于水的电离,在pH=11的K2CO3溶液中,c(H+)=10-11 mol/L,是CO32-结合剩余的,而c(OH-)=10-3 mol/L是水电离出的全部,故由水电离出来c(OH-)是10-23mol/L.
故答案为:10-3.
点评 本题考查了离子积常数的有关计算,明确酸或碱抑制水电离、含有弱根离子的盐促进水电离是解本题关键,注意碱中氢氧根离子浓度不等于水电离出氢氧根离子浓度,为易错点.


 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:解答题
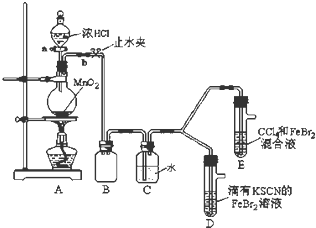
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯. | D装置中:溶液变红 E装置中:水层溶液变黄,振荡后,下层CCl4层无明显变化. | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为: Cl2>Br2>Fe3+ |
| ⅰ.Fe3++3SCN-?Fe(SCN)3 是一个可逆反应. ⅱ.(SCN)2性质与卤素单质类似.氧化性:Cl2>(SCN)2. ⅲ.Cl2和Br2反应生成BrCl,BrCl呈红色(略带黄色),沸点约5℃,它与水能发生水解反应,且该反应为非氧化还原反应. ⅳ.AgClO、AgBrO均可溶于水. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
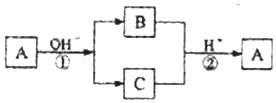
| A. | X元素可能为Al | B. | X元素可能为金属,也可能为非金属 | ||
| C. | 反应①和②互为可逆反应 | D. | 反应①和②一定为氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 | |
| B. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 | |
| C. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 | |
| D. | 防止酸雨发生的重要措施之一是使用清洁能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20℃,1.01×105Pa下 11.2LN2含有的分子数为3.01×1023 | |
| B. | 4℃时9mL水和标准状况下11.2L氮气含有相同的分子数 | |
| C. | 同温同压下,lmol NO与lmol N2和O2的混合气体的体积不相等 | |
| D. | 0℃、1.01×10sPa时,11.2L氧气所含的原子数目为3.01×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,20mL NH3跟60mL O2所含的分子个数比为1:3 | |
| B. | 22.4L O2中一定含有6.02×1023个氧分子 | |
| C. | 将80克NaOH溶于1L水中,所得溶液的物质的量浓度为2mol/L | |
| D. | 18克H2O在标准状况下的体积为0.018L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶未干燥 | |
| B. | 定容时俯视液面 | |
| C. | 转移时有液体溅出 | |
| D. | 颠倒摇匀后发现液面低于刻度线,再加水至刻度线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com