
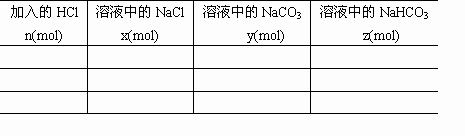
取0.45mol NaOH、0.35mol Na2CO3和0.20mol NaHCO3溶解于水,该混合液中逐渐加入盐酸,反应明显分三个段进行.若加入的HCl为n mol,溶液中NaCl、Na2CO3、NaHCO3分别为x mol、y mol、z mol,试分别计算在n值增大的过程中,不同反应阶段的n值范围和所对应的x、y、z值.将其结果填入下表.(提示:Na2CO3+HCl![]() NaHCO3+NaCl,NaHCO3+HCl
NaHCO3+NaCl,NaHCO3+HCl![]() NaCl+H2O+CO2↑)
NaCl+H2O+CO2↑)
|
分析: 当三种物质溶于水,立即发生如下的反应: NaOH+NaHCO3 三种物质,物质的量将发生如下变化: NaOH 0.45-0.20=0.25(mol) NaHCO3 0.20-0.20=0 Na2CO3 0.35+0.20=0.55(mol) 当向溶液中逐步加入盐酸时,反应明显分三步进行: (1)NaOH+HCl (2)Na2CO3+HCl (3)NaHCO3+HCl 由反应可知消耗HCl的量就是生成NaCl的量(Cl元素守恒).溶液中NaOH、Na2CO3、NaHCO3的量随HCl物质的量n mol改变而变化.
|


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:高中化学习题1 题型:022
取0.45mol ![]() 、0.35mol
、0.35mol ![]() 、0.20mol
、0.20mol ![]() 溶解于水,在该混合溶液中加入盐酸,反应明显分为三个阶段进行.若加入的盐酸为n mol,溶液中
溶解于水,在该混合溶液中加入盐酸,反应明显分为三个阶段进行.若加入的盐酸为n mol,溶液中![]() 、
、![]() 和
和![]() 分别为x mol,y mol和z mol.试分别计算在n值增大过程中,不同反应阶段的n值范围和所对应的x、y、z值.将其结果填入下表.
分别为x mol,y mol和z mol.试分别计算在n值增大过程中,不同反应阶段的n值范围和所对应的x、y、z值.将其结果填入下表.
提示:![]() 与
与![]() 的反应过程为:
的反应过程为:
①![]()
![]()
![]()
②![]()
![]()
![]()

查看答案和解析>>
科目:高中化学 来源:知识精讲与能力训练 高三化学 题型:038
取0.45mol NaOH、0.35mol Na2CO3和0.29mol NaHCO3溶解于水,在该混合液中逐渐加入盐酸,反应明显分三个阶段进行.若加入的HCl为n mol,溶液中NaCl、Na2CO3和NaHCO3分别为x mol、y mol和z mol,试分别试算在n值增大的过程中,不同反应阶段的n值范围和对应的x,y,z值.将其结果填入下表.(提示:Na2CO3和HCl的反应过程为:1.Na2CO3+HCl=NaHCO3+NaCl,
2.NaHCO3+HCl=NaCl+H2O+CO2↑)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com