
【题目】有机物A由碳、氢、氧三种元素组成.现取2.3g A与2.8L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余).将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7g,碱石灰增重2.2g.回答下列问题:
(1)2.3g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式.
【答案】
(1)解:n(O2)= ![]() =0.125 mol,则 m(O2)=0.125 mol×32gmol﹣1=4 g,
=0.125 mol,则 m(O2)=0.125 mol×32gmol﹣1=4 g,
故m(CO)=4 g+2.3 g﹣2.7 g﹣2.2 g=1.4 g,
n(CO)= ![]() =0.05 mol,
=0.05 mol,
n(H2O)= ![]() =0.15 mol,
=0.15 mol,
n(CO2)= ![]() =0.05 mol,
=0.05 mol,
则n(H)=2n(H2O)=0.15 mol×2=0.3 mol
n(C)=n(CO2)+n(CO)=0.05 mol+0.05 mol=0.1 mol
答:2.3 g A中所含氢原子、碳原子的物质的量分别为0.3 mol 和0.1 mol
(2)解:2.3 g A中所含氧原子:n(O)=(0.05 mol×2+0.05 mol+0.15 mol)﹣0.125 mol×2=0.05 mol,
n(C):n(H):n(O)=0.1 mol:0.3 mol:0.05 mol=2:6:1
则A的最简式为 C2H6O,根据价键规则A的分子式为 C2H6O,
答:A 的分子式为 C2H6O
【解析】浓硫酸增重为水的质量,碱石灰增重为二氧化碳的质量,根据质量守恒计算CO的质量,再根据原子守恒计算分子中C、H、O原子物质的量,进而确定有机物最简式,若最简式中H原子已经饱和碳的四价结构,则最简式即为分子式,否则需要知道相对分子质量确定分子式.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】糖类、油脂及蛋白质是基本营养物质。下列说法正确的是
A.都是高分子化合物
B.均只含C、H、O三种元素
C.油脂发生皂化反应后可以制得肥皂
D.在人体中消耗相同质量的上述三种物质时,蛋白质产生的能量最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,混合物中含有物质A和B,已知A为黑色粉末,B为白色粉末,发生如下变化:
(1)写出下列各物质的化学式:A , B , C , D , G .
(2)写出①、②、③、④四处变化的化学方程式:①;
②;
③;
④ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.能使广泛pH试纸显蓝色的溶液:K+、Na+、CH3COO﹣、Br﹣
B.甲基橙呈红色的溶液:NH4+、Ba2+、AlO ![]() 、Cl﹣
、Cl﹣
C.0.1 molL﹣1 FeCl3溶液:K+、NH![]() 、I﹣、SCN﹣
、I﹣、SCN﹣
D.由水电离的c (H+)=1×10﹣14 molL﹣1的溶液中:Ca2+、K+、Cl﹣、HCO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷广泛存在于天然气、沼气、煤矿坑气之中,是优质的气体燃料,更是制造许多化工产品的重要原料.
(1)制取氢气
已知:CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206.2kJmol﹣1
CH4(g)+CO2(g)2CO(g)+2H2(g)△H=+247.4kJmol﹣1
(i)请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式
(ii)若将0.1mol CH4和0.1mol H2O(g)通入体积为10L的密闭容器里,在一定条件下发生反应:
CH4(g)+H2O(g)CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率
②该反应的化学平衡常数;
③图中的p1p2(填“<”、“>”或“=”);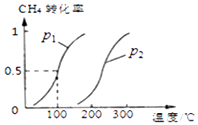
(2)制备甲醇
在压强为0.1MPa条件下,将a mol CO与3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)CH3OH(g)△H<0.若容器容积不变,下列措施可增加甲醇产率的是
A.升高温度
B.再充入1mol CO和3mol H2
C.将CH3OH(g)从体系中分离
D.充入He,使体系总压强增大
E.使用更高效的催化剂
(3)合成乙酸
甲烷直接合成乙酸具有重要的理论意义和应用价值.光催化反应技术使用CH4和(填化学式)直接合成乙酸,且符合“绿色化学”的要求(原子利用率100%).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种工业原料。工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
A.若管道漏气遇氨会产生白烟
B.该反应利用了氯气的强氧化性
C.该反应属于复分解反应
D.生成1 mol N2有6 mol电子转移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com