
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的H2O与D2O含有的中子数 | |
| B. | 等质量的SO2和SO3中含有氧原子数 | |
| C. | 同温同压下,同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别于足量氯气完全反应时转移的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
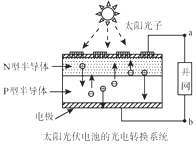 世博会中国馆、主题馆等建筑所使用的光伏电池,总功率达4兆瓦,是历届世博会之最.下列有关叙述正确的是( )
世博会中国馆、主题馆等建筑所使用的光伏电池,总功率达4兆瓦,是历届世博会之最.下列有关叙述正确的是( )| A. | 电流从a流向b | |
| B. | N型半导体为正极,P型半导体为负极 | |
| C. | 光伏电池是将化学能转变为电能 | |
| D. | 光伏电池是将太阳能转变为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,SO2(g)和O2(g)所具有的能量大于SO3(g)所具有的能量 | |
| B. | 将2molSO2(g)和O2(g)置于某密闭容器中充分反应,放出热量为QkJ | |
| C. | 增大压强或升高温度,该平衡都向正反应方向移动 | |
| D. | 若将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QkJ,则此过程有2molSO2(g)被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | 一定条件下,Z单质与W的常见单质直接生成ZW | |
| B. | X最高价氧化物对应的水化物与Y的最高价氧化物对应的水化物能反应 | |
| C. | Y的最高价氧化物对应的水化物不能溶于稀氨水 | |
| D. | 一定条件下,w单质可以将z单质从其氢化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [C2O42-]>0.63[CO32-] | B. | [C2O42-]>1.6[CO32-] | ||
| C. | [C2O42-]<1.6[CO32-] | D. | [C2O42-]<0.63[CO32-] | ||
| E. | 无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com