
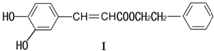
| A. | 遇FeCl3溶液可能显紫色 | |
| B. | 可发生酯化反应和银镜反应 | |
| C. | 能与溴发生取代和加成反应 | |
| D. | 1mol化合物I最多能与2molNaOH反应 |
分析 该有机物中含有苯环、酚羟基、碳碳双键和酯基,具有苯、酚、烯烃和酯的性质,能发生加成反应、还原反应、取代反应、氧化反应、显色反应、加聚反应、水解反应等,据此分析解答.
解答 解:A.含有酚羟基,所以具有酚的性质,能与氯化铁溶液发生显色反应,故A正确;
B.不含醛基,所以不能发生银镜反应,故B错误;
C.含有酚羟基且苯环上酚羟基邻对位含有氢原子,含有碳碳双键,所以能与溴发生取代反应和加成反应,故C正确;
D.酚羟基和酯基水解生成的羧基能与氢氧化钠反应,所以1mol化合物I最多能与3molNaOH反应,故D错误;
故选AC.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酚、烯烃性质,注意苯酚和溴发生取代反应时的取代位置,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①④ | B. | 只有③ | C. | 只有②③ | D. | 只有①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCO3溶液(NaHCO3),选用适量NaOH溶液 | |
| B. | NaHCO3溶液(NaCO3),应通入过量CO2气体 | |
| C. | Na2O2粉末(Na2O),将混合物在空气中加热 | |
| D. | 镁粉(铝粉),选用过量的烧碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
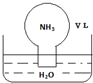
| A. | 水最终会充满整个烧瓶 | |
| B. | 所得溶液的物质的量浓度为$\frac{1}{22.4}$ mol•L-1 | |
| C. | 所得溶液的质量分数为$\frac{17}{22400}$ρ | |
| D. | 所得溶液中,n(NH3•H2O)+n(NH4+)=$\frac{V}{22.4}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=5的NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| B. | 在0.1mol•L-1 CH3COONa溶液中:n(OH-)+0.1mol>n(CH3COOH)+n(H+)+n(Na+) | |
| C. | 向AgBr的饱和溶液中加入NaCl固体,有白色固体析出,说明AgCl比AgBr更难溶 | |
| D. | 10mL 0.01mol•L-1 H2SO4溶液与10mL 0.01mol•L-1 NaOH溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 mol/(L•s) | B. | 0.16 mol/(L•s) | C. | 0.32mol/(L•s) | D. | 0.8 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com