
| A. | 氢氧化钠溶液与醋酸反应 | B. | 氢氧化钙与稀盐酸反应 | ||
| C. | 氢氧化钡与稀硫酸反应 | D. | 氢氧化钾与稀硝酸反应 |
分析 H++OH-═H2O表示强酸或者强酸的酸式盐与可溶性强碱反应生成水和可溶性盐,据此解答.
解答 解:A.醋酸为弱酸,应保留化学式,所以氢氧化钠溶液与醋酸反应不能用H++OH-═H2O表示,故A错误;
B.氢氧化钙乳浊液中氢氧化钙应保留化学式,所以氢氧化钙与稀盐酸反应不一定能用H++OH-=H2O表示,故B错误;
C.反应除了生成水还生成硫酸钡沉淀,所以反应不能用H++OH-═H2O表示,故C错误;
D.反应实质为氢离子与氢氧根离子生成水,离子方程式:H++OH-=H2O,故D正确;
故选:D.
点评 本题考查了离子方程式书写,明确离子方程式意义及离子方程式书写方法是解题关键,题目难度不大,注意化学式的拆分.


科目:高中化学 来源: 题型:多选题
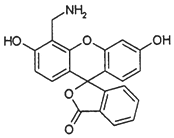
| A. | 分子中三个苯环处于同一平面 | |
| B. | 1 mol 4-AFMF 最多可与2molNaOH 反应 | |
| C. | 在酸性条件下水解,水解产物只有1种 | |
| D. | 能与溴水、FeCl3溶液及稀硫酸发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 | |
| 平衡时数据 | 反应能量变化的绝对值(kJ) | Q1 | Q2 | Q3 |
| 反应物转化率 | a1 | a2 | a3 | |
| 体系压强(Pa) | p1 | P2 | P3 | |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH+HCl | B. | Ba(OH)2+H2SO4 | C. | Fe(OH)3+HNO3 | D. | KOH+H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氨在工农业生产中应用广泛.在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如表:
氨在工农业生产中应用广泛.在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如表:| 温度/℃ | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCN的结构式:H-C≡N | |
| B. | HClO的电子式: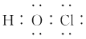 | |
| C. | 质子数为86、中子数为51的铯原子:86137Cs | |
| D. | S2-的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体中含有的碳碳双键数为NA | |
| B. | 混合气体中含有的碳原子数为2NA | |
| C. | 当混合气体完全燃烧时,消耗O2的分子数为3NA | |
| D. | 当混合气体完全燃烧时,转移的电子数为12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
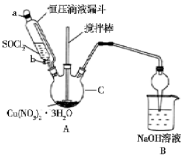 硝酸铜是一种重要的化工原料,实验室以含铁的铜屑为原料制备硝酸铜的过程如下,请按要求回答问题
硝酸铜是一种重要的化工原料,实验室以含铁的铜屑为原料制备硝酸铜的过程如下,请按要求回答问题| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO、ClO2、SO2都属于氧化物 | |
| B. | 液氯、铁单质、液态氯化氢都属于电解质 | |
| C. | 能发生丁达尔效应的分散系有NaCl溶液、水、蛋白质溶液等 | |
| D. | 除去氢氧化铁胶体中的Na+和Cl-可用过滤的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com