解:(1)某非金属元素A的氧化物B能与NaOH溶液反应生成盐C的溶液,向C的溶液中加入过量盐酸,生成沉淀D,可知A为Si,B为SiO
2,C为Na
2SiO
3,D为H
2SiO
3,C与盐酸反应生成D的离子方程式是SiO
32-+2H
+=H
2SiO
3↓,
故答案为:SiO
32-+2H
+=H
2SiO
3↓;
(2)向A的水溶液中滴入品红试液,品红褪色,将溶液加热后,溶液颜色无明显变化,应为Cl
2,向B的水溶液中滴入品红试液,品红褪色,将溶液加热后,溶液又呈红色,应为SO
2,向C的水溶液中滴入红色石蕊试液,溶液呈蓝色,应为NH
3,
①将适量的A通入B的水溶液中发生反应的化学方程式是Cl
2+SO
2+2H
2O=2HCl+H
2SO
4,二者发生氧化还原反应,故答案为:Cl
2+SO
2+2H
2O=2HCl+H
2SO
4;
②工业常用氨气的催化氧化法制备硝酸,即C生成D的反应,反应的方程式为4NH
3+5O
2
4NO+6H
2O,
故答案为:4NH
3+5O
2 
4NO+6H
2O.
分析:(1)某非金属元素A的氧化物B能与NaOH溶液反应生成盐C的溶液,向C的溶液中加入过量盐酸,生成沉淀D,可知A为Si,B为SiO
2,C为Na
2SiO
3,D为H
2SiO
3;
(2)向A的水溶液中滴入品红试液,品红褪色,将溶液加热后,溶液颜色无明显变化,应为Cl
2,向B的水溶液中滴入品红试液,品红褪色,将溶液加热后,溶液又呈红色,应为SO
2,向C的水溶液中滴入红色石蕊试液,溶液呈蓝色,应为NH
3.
点评:本题考查无机物的推断,题目难度不大,注意根据物质反应的现象最为解答的突破口,牢固把握相关物质的性质为解答该类题目的关键.

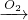 D
D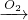 E
E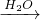 F,则C→D反应的化学方程式为______.
F,则C→D反应的化学方程式为______. 4NO+6H2O,
4NO+6H2O, 4NO+6H2O.
4NO+6H2O.