

| 容器编号 | c(CO)/mol.L-1 | c(O2)/mol.L-1 | (CO2)/mol.L-1 | v(正)和v(逆)比较 |
| Ⅰ | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | v(正)>v(逆) |
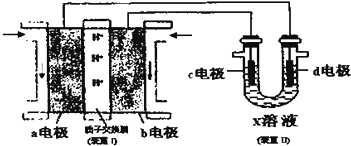
分析 (1)碳和二氧化碳反应生成一氧化碳;碳与水蒸气和碳与二氧化碳反应是吸热反应;
(2)再利用II中的Q来判断反应进行的方向,从而得出正逆反应速率的关系;
(3)根据流程图可知甲烷不完全燃烧生成一氧化碳和氢气,依据热化学方程式的书写方法写出,标注物质聚集状态和对应焓变;
(4)①根据v=$\frac{△c}{△t}$进行计算;
②反应速率加快,而且在t的时刻,达平衡状态进行分析求解;
③平衡正向移动,是增加CO的量导致平衡正向移动;
(5)①由装置II中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg可知,d极为阳极,而c极为阴极;
②根据阳极产生气体的体积,求出整个过程中转移电子的物质的量,然后铜的相对原子质量.
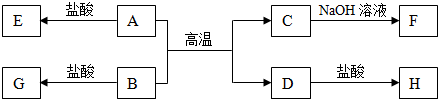
解答 解:(1))碳和二氧化碳反应生成一氧化碳,方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO;碳与水蒸气和碳与二氧化碳反应是吸热反应,所以①③的变化过程是吸热反应,故答案为:C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO;①③;
(2)由Ⅰ可求K=$\frac{4×1{0}^{-2}}{2×1{0}^{-4}\sqrt{4.0×1{0}^{-4}}}$=104,
由Ⅱ可求Q=$\frac{5.0×1{0}^{-2}}{3.0×1{0}^{-4}\sqrt{4.0×1{0}^{-4}}}$=$\frac{5}{6}$×104<K,
故平衡右移,v(正)>v(逆),故答案为:>;
(3)根据流程图可知甲烷不完全燃烧生成一氧化碳和氢气,1gCH4燃烧生成一氧化碳和氢气放热2.21kJ,16g甲烷燃烧生成二氧化碳和液态水放出热量16×2.21kJ=35.36KJ,16g甲烷为1mol,则甲烷不完全燃烧的热化学方程式为:2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=-70.72 kJ•mol-1,
故答案为:2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=-70.72 kJ•mol-1;
(4)①根据v=$\frac{△c}{△t}$=$\frac{\frac{2-1.6}{2}}{t}$=$\frac{1}{5t}$mol/(L•min),故答案为:$\frac{1}{5t}$mol/(L•min);
②反应速率加快,而且在t的时刻,达平衡状态,可能是反应受热或使用了催化剂,故答案为:反应受热或使用了催化剂;
③平衡正向移动,是增加CO的量导致平衡正向移动,所以图象为: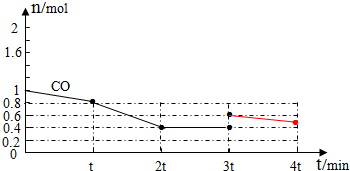 ,故答案为:
,故答案为: ;
;
(5)①由装置II中某电极上收集到标准状况下的气体V1mL时,另一电极增重mg可知,d极为阳极,而c极为阴极,所以与d极相连的a极为正极,原电池中阳离子向正极移动,b电极为负极是燃料发生氧化反应,反应方程式为:CH3OH-6eˉ+H2O=CO2+6H+,故答案为:a、CH3OH-6eˉ+H2O=CO2+6H+;
②整个过程中转移电子的物质的量为:$\frac{1{0}^{-3}{V}_{1}}{22.4}$,所以生成铜的物质的量为:$\frac{{V}_{1}}{11200}$,所以铜的相对原子质量的表达式为$\frac{11200m}{{V}_{1}}$,故答案为:$\frac{11200m}{{V}_{1}}$.
点评 本题考查溶度积、化学反应热、平衡的移动和电化学的相关知识,综合性强,有难度,注意知识的梳理和整合是解题的关键.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:解答题
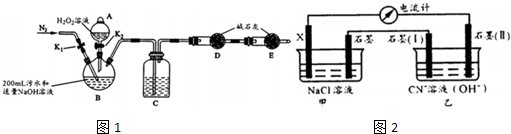
| 步骤1 | 关闭K1,打开K2,滴入足量H2O2溶液,对B加热.充分反应后,停止加热 |
| 步骤2 | 关闭K2,用注射器穿过B装置的胶塞注入 稀H2S04溶液 |
| 步骤3 | 打开K1,通入N2 |
| 实验序号 | 电极(X) | NaCl溶液浓度 (mol/L) | 甲中石墨表面通入气体 | 电流计读数 (A) |
| (1) | Fe | 0.1 | 空气 | I |
| (2) | Al | 0.1 | 空气 | 1.5I |
| (3) | Fe | 0.1 | O2 | 2I |
| (4) | Al | 0.5 | 空气 | 1.6I |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.25 mol•L-1 | B. | 0.025 mol•L-1 | C. | 0.5 mol•L-1 | D. | 0.125 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在海带灰的滤液中加入几滴稀硫酸,再加入双氧水,即能使淀粉溶液变蓝2I-+H2O2+2H+═I2+2H2O | |
| B. | Na2S2O3溶液中加入稀硫酸:2S2O32-+2H+═SO42-+3S↓+H2O | |
| C. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ | |
| D. | 在AgCl饱和溶液在加入Na2S:2Ag++S2-═Ag2S↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com