
【题目】高聚物的合成与结构修饰是制备具有特殊功能材料的重要过程。下图是合成具有特殊功能高分子材料W(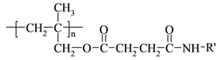 )的流程:
)的流程:
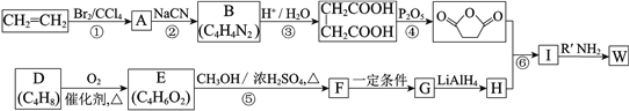
已知:(R、R1、R2代表烃基)
I、![]()
![]() RCH2OH
RCH2OH
II、![]()
⑴反应①的反应类型是_______________。
⑵反应②是取代反应,其化学方程式是___________________________________________。
⑶D的核磁共振氢谱中有两组峰且面积之比是1:3,不存在顺反异构。D的结构简式是______。
⑷反应⑤的化学方程式是__________________________________________________。
⑸G的结构简式是__________________。
⑹反应⑥的化学方程式是__________________________________________________。
⑺工业上也可用![]() 合成E。由上述①~④的合成路线中获取信息,完成下列合成路线(箭头上注明试剂和反应条件,
合成E。由上述①~④的合成路线中获取信息,完成下列合成路线(箭头上注明试剂和反应条件, 不易发生取代反应)__________________
不易发生取代反应)__________________
![]()
【答案】 加成反应 BrCH2CH2Br +2NaC→ NCCH2CH2CN + 2NaBr (CH3)2C=CH2 CH2=C(CH3)COOH + HOCH3 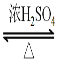 CH2=C(CH3)COOCH3 + H2O
CH2=C(CH3)COOCH3 + H2O 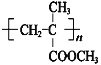
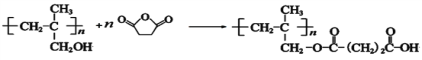
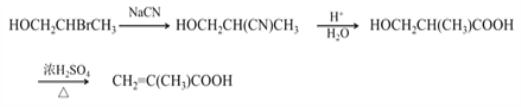
【解析】根据反应条件![]() ,结合W的结构
,结合W的结构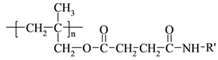 可知I为
可知I为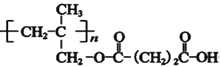 ,由此可知H为
,由此可知H为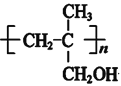 ,再结合信息I可知G为
,再结合信息I可知G为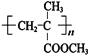 ,相应的单体F为CH2=C(CH3)COOCH3,E和CH3OH酯化反应得到F,则E的结构为CH2=C(CH3)COOH;
,相应的单体F为CH2=C(CH3)COOCH3,E和CH3OH酯化反应得到F,则E的结构为CH2=C(CH3)COOH;
⑴反应①是乙烯与Br2发生加成反应生成BrCH2CH2Br;
⑵反应②BrCH2CH2Br与NaCN发生取代反应生成NCCH2CH2CN,其化学方程式是 BrCH2CH2Br +2NaCN→ NCCH2CH2CN + 2NaBr;
⑶C4H8的核磁共振氢谱中有两组峰且面积之比是1:3,说明有2个甲基,且不存在顺反异构,说明不饱和碳上连有相同基团,则D的结构简式是(CH3)2C=CH2;
⑷反应⑤是CH2=C(CH3)COOH 与 HOCH3发生的酯化反应,其化学方程式是CH2=C(CH3)COOH + HOCH3 ![]() CH2=C(CH3)COOCH3 + H2O ;
CH2=C(CH3)COOCH3 + H2O ;
⑸G的结构简式是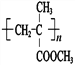 ;
;
⑹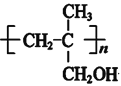 和
和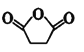 发生反应的化学方程式是
发生反应的化学方程式是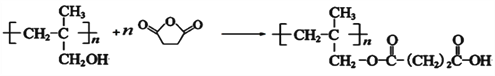 ;
;
⑺结合①~④的合成路线中获取信息,用![]() 合成CH2=C(CH3)COOCH3 的流程为
合成CH2=C(CH3)COOCH3 的流程为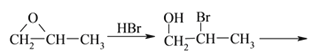
![]()
![]()
![]() 。
。


科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1的NaOH溶液分别滴定体积均为50.00mL、浓度均为0.05mol·L-1的HClO、HF两种溶液,其滴定曲线如图所示。
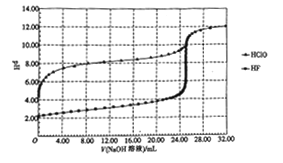
下列说法正确的是
A. HClO的酸性比HF强
B. V(NaOH溶液)=0 mL 时,对应溶液中:c(ClO-)=c(F-)
C. V(NaOH溶液)=12.50 mL 时,对应溶液中:c(ClO-)>c(F-)
D. V(NaOH溶液)=25.00mL时,对应溶液中:c(ClO-)<c(F-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则x值为( )(要求写出解答过程)
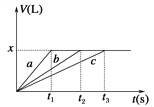
A. 1.12 B. 4.48
C. 2.24 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
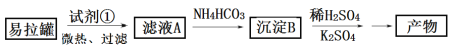
(1)为尽量少引入杂质,试剂①应选用___(填标号)。
a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为________。
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是__________。
(4)已知:Kw=1.0×10-14,Al(OH)3![]() AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解装置如图所示:
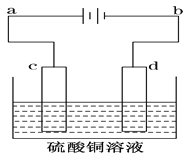
Ⅰ.当用惰性电极电解时,c为____________极,电极反应________d为____________极,电极反应______________,电解总反应的化学方程____________________
Ⅱ.(1)若用此装置进行铁上镀铜则c为__________(填铁或铜)d为___________(填铁或铜)电解液浓度_____________(增大,减小或不变)
(2)电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子___________mol.
Ⅲ.若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极________(填图中的字母);若粗铜中还含有Au、Ag、Fe,则Fe以_______(填离子符号)形式进入溶液,c电极发生的反应______________,________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质发生变化时,所克服的微粒间作用力属于同种类型的是( )
A.二氧化硅和氢氧化钠的熔化
B.碘和干冰的升华
C.氯化氢和氯化钠的溶解
D.汞和硫的气化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有如下两个反应:(1)Cu+2Fe3+=Cu2++2Fe2+(2)Fe+Cu2+=Fe2++Cu。判断Fe3+、Fe2+、Cu2+氧化性强弱顺序排列正确的是
A. Fe3+>Cu2+>Fe2+
B. Cu2+>Fe3+>Fe2+
C. Fe3+Fe2+>Cu2+
D. Fe2+>Cu2+>Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用无机矿物资源生产部分材料。下列有关说法不正确的是
A.制取玻璃的同时产生CO2气体,制取粗硅时生成的气体产物为CO
B.生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应
C.粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法
D.黄铜矿(CuFeS2)冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学实验操作、现象及结论均正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 取1 mL 20%的蔗糖溶液,加入3~5滴稀硫酸,水浴加热一段时间后,再滴加银氨溶液 | 没有出现银镜 | 蔗糖没有水解 |
B | 锅炉中的水垢用饱和碳酸钠溶液浸泡后,再加入稀盐酸 | 水垢明显减少 | 锅炉沉积物中的CaSO4转化为CaCO3 |
C | 常温下,在0.1 mol·L1氨水中,加入少量NH4Cl晶体 | 溶液的pH减小 | NH4Cl溶液显酸性 |
D | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | NaHCO3为难溶物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com