铜及其化合物在生产生活中有着广泛的应用,铜在化合物中的常见化合价有+l、+2.
(1)工业上可用Cu
2S+O
22Cu+SO
2反应制取粗铜,反应中被氧化的元素是
,当有32gCu
2S消耗时,电子转移数目是
.
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H
2O
2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,温度控制在50℃-60℃的两个原因除了加快反应速率外,还有
.在CuSO
4溶液中加入一定量的Na
2SO
3和NaCl溶液加热,生成CuCl沉淀,写出生成CuCl的离子方程式
.
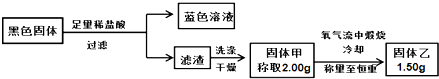
(3)某小组同学在做铜与浓硫酸反应的实验时,发现铜片表面有黑色固体生成.
①甲同学猜想:黑色固体是未来得及溶解于酸的CuO,其猜想可用化学方程式表示为:
Cu+H
2SO
4
.
②乙同学认为:黑色固体除CuO外还可能含有Cu
2S和CuS.其理由可能是
(填字母)
a.Cu
2S和CuS都是黑色的 b.铜与浓硫酸在加热条件下反应,还可能放出O
2c.浓硫酸是氧化剂,铜是还原剂,Cu的化合价上升与S的化合价下降有多种可能
(4)用一定量的铁与足量的稀H
2SO
4及足量的CuO制成单质铜,有人设计以下两种方案:
①Fe
H
2Cu ②CuO
CuSO
4Cu
若按实验原则进行操作,则两者制得单质铜的量的比较中,正确的是
(填字母)
A.①多 B.②多 C.相等 D.无法判断.