
【题目】下列物质中,既含离子键、又含极性共价键的是( )
A.NaOH
B.Na2O
C.HCl
D.CaCl2
科目:高中化学 来源: 题型:
【题目】用2mL 1mol·L-1CuSO4溶液与3mL 0.5mol·L-1NaOH溶液混合后,加入40%的甲醛溶液0.5mL,加热至沸腾,无红色沉淀生成,实验失败的主要原因是
A. 甲醛的量太少 B. CuSO4的量太多
C. NaOH的量太少 D. 加热的时间太短
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度℃ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______(用K1、K2表示)。500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15, 则此时 V正_____ V逆(填“ > ”、“=”或“<”)。
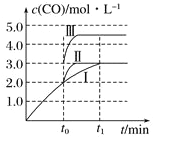
(2)在3 L容积可变的密闭容器中发生反应②,已知c(CO)-反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是______________。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是_________________。
(3)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下, 将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为________________。
(Ⅱ)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。
(1)常温下,向10 mL 0.01 mol·L-1 H2C2O4溶液中滴加10mL 0.01mol·L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系_________________________ ;
(2)称取6.0g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解配成250 mL 溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。第一份溶液中加入2滴酚酞试液,滴加0.25mol·L-1 NaOH 溶液至20mL时,溶液由无色变为浅红色。第二份溶液滴加0.10 mol·L-1 酸性KMnO4溶液至16mL时反应完全。则原试样中H2C2O4·2H2O的的质量分数为_______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关天然产物水解的叙述不正确的是
A. 纤维素水解与淀粉水解得到的最终产物不同
B. 可用碘检验淀粉水解是否完全
C. 蛋白质水解的最终产物均为氨基酸
D. 油脂水解可得到丙三醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是 ( )
A. 金属的电化腐蚀比化学腐蚀普遍
B. 钢铁在干燥空气里不易腐蚀
C. 用铝质铆钉接铁板,铁板易被腐蚀
D. 原电池电路中电子由负极流入正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200 mL 1 mol/L的氯化铝溶液中加入一定体积的2 mol/L的NaOH溶液,最终产生7.8 g沉淀,则加入的NaOH溶液的体积可能是( )
① 350 mL ② 90 mL ③ 150 mL ④200 mL
A. 只有① B. ①③ C. ②④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)性能优越,被称为继铁、铝制后的“第三金属”。工业上以金红石为原料制取Ti的反应为:
aTiO2+bCl2+cC ![]() aTiCl4+cCO ……反应I
aTiCl4+cCO ……反应I
TiCl4+2Mg![]() Ti+2MgCl2 ……反应II
Ti+2MgCl2 ……反应II
关于反应I、II的分析不正确的是 ( )
① TiCl4在反应I中是还原产物,在反应II中是氧化剂;
② C、Mg在反应中均为还原剂,被还原;
③ 在反应I、II中Mg的还原性大于Ti,C的还原性大于TiCl4;
④ a=1,b=c=2;
⑤ 每生成0.1molTi,反应I、II中共转移0.4mole-。
①②④ B.②③④ C.② D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用H++OH-=H2O来表示的化学反应是( )。
A.CH3COOH+NaOH==CH3COONa+H2O
B.HNO3+KOH=KNO3+H2O
C.H2SO4+Ba(OH)2=BaSO4↓+2H2O
D.2HCl+Cu(OH)2=CuCl2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用 FeCl3 溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL 废液加入足量的 AgNO3 溶液,生成沉淀 8.61g。(2)另取 10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液组成的判断错误的是
A. 一定含有 Fe 2+、 Fe 3+、 Cu2+、 Clˉ B. c(Fe2+):c(Cu2+) = 2:1
C. c(Clˉ) = 6mol / L, c(Fe 2+) = 1.2mol / L D. c (Fe2+):c(Fe 3+) = 3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com