
| 104×92.3% |
| 12 |
| 104-12×8 |
| 1 |
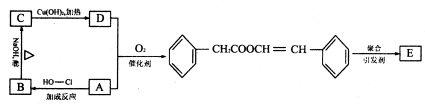
 结合题中各物质转化关系,可知A为
结合题中各物质转化关系,可知A为 ,A发生加成反应生成B,所以B为
,A发生加成反应生成B,所以B为 ,B在氢氧化钠醇溶液中发生消去反应生成C,所以C为
,B在氢氧化钠醇溶液中发生消去反应生成C,所以C为 ,C被氧化成D,所以D为
,C被氧化成D,所以D为 ,
, 发生加聚反应生成E,所以E为
发生加聚反应生成E,所以E为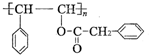 ,据此答题;
,据此答题;| 104×92.3% |
| 12 |
| 104-12×8 |
| 1 |
 结合题中各物质转化关系,可知A为
结合题中各物质转化关系,可知A为 ,A发生加成反应生成B,所以B为
,A发生加成反应生成B,所以B为 ,B在氢氧化钠醇溶液中发生消去反应生成C,所以C为
,B在氢氧化钠醇溶液中发生消去反应生成C,所以C为 ,C被氧化成D,所以D为
,C被氧化成D,所以D为 ,
, 发生加聚反应生成E,所以E为
发生加聚反应生成E,所以E为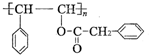 ,
, ,
, ;
; ,
, (其中两种);
(其中两种);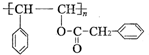 ,
,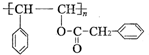 ;
;


科目:高中化学 来源: 题型:
| A、SO3溶于水后能导电,故SO3为电解质 |
| B、强电解质的水溶液中不存在大量溶质分子 |
| C、向NaCN溶液中滴入酚酞试液显红色,则HCN为强酸 |
| D、25℃时,用CH3COOH溶液滴定等浓度NaOH溶液至pH=7,V(CH3COOH)<V(NaOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
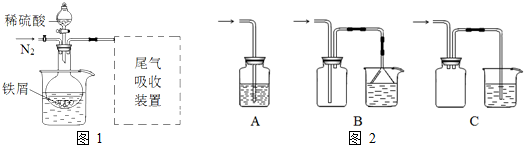
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常用丁达尔效区分溶液与胶体 |
| B、在铜锌原电池中,负极上发生Zn-2e-═Zn2+ |
| C、常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均减少 |
| D、向AgCl沉淀中滴加KI溶液,沉淀变为黄色,说明Ksp(AgCl)>Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 测定序号 | 待测溶液的体积/mL | 所耗盐酸标准液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.50 |
| 2 | 20.00 | 1.20 | 21.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
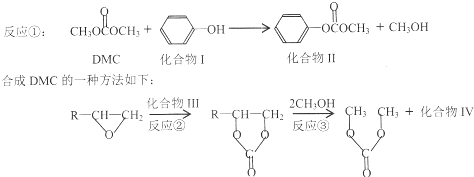
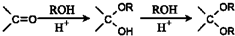
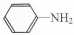 与DMC1:1发生类似反应①的反应,请写出反应方程式
与DMC1:1发生类似反应①的反应,请写出反应方程式查看答案和解析>>
科目:高中化学 来源: 题型:
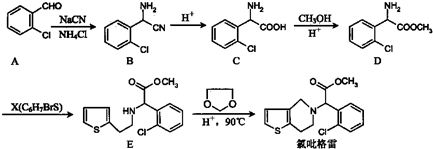
 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com