
某化学兴趣小组为了探究:在常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1: ;猜想2 ;猜想3 。
为了验证猜测,该小组设计实验加以探究:
[实验探究]
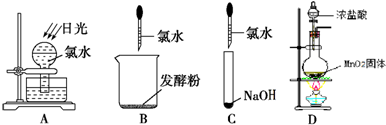
该小组同学按如图所示装置,将气体从a端通入:
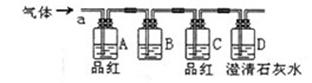
(1)B中应该装下列 试剂(填编号);
A.NaCl溶液 B.KMnO4溶液 C.浓溴水 D.饱和NaHCO3溶液
(2)A中品红的作用是: ;
(3)D中澄清石灰水的作用是: 。
通过该实验,小组同学观察到以下三个实验现象:
①A中品红褪色 ②C中品红不褪色 ③D中澄清石灰水变浑浊
[得出结论]
由上述现象小组同学确认该气体的成分是 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组为了探究在常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.
某化学兴趣小组为了探究在常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com