
| A、4.6g组成为C2H6O的有机物,所含C-H键数目一定为0.6NA |
| B、12g金刚石中含有的共价键数为2NA |
| C、0.1mol的白磷(P4)或甲烷中所含的σ键数均为0.4NA |
D、0.5mol雄黄(As4S4结构如图)含有NA个S-S键 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
| A、盐酸、天然气、醋酸、干冰 |
| B、胆矾、漂白粉、氯化钾、氯气 |
| C、氯化钠、福尔马林、硫酸钠、乙醇 |
| D、单甘油酯、混甘油酯、苛性钾、石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
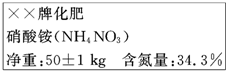
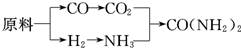
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S(g)+O2(g)═SO2(g)|△H|=297.23 kJ?mol-1 |
| B、S(g)+O2(g)═SO2(g)|△H|<297.23 kJ?mol-1 |
| C、1 mol SO2(g)所具有的能量大于1 mol S(s)与1 mol O2(g)所具有的能量之和 |
| D、1 mol SO2(g)所具有的能量小于1 mol S(s)与1 mol O2(g)所具有的能量之和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
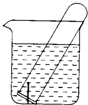 如图水槽中试管内有一枚铁钉,放置数天后观察:
如图水槽中试管内有一枚铁钉,放置数天后观察:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/LNH4Cl溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、pH=2的HCl溶液与pH=12的NaOH溶液等体积混合所得溶液中:c(Na+)=c(Cl-)>c(OH-)=c(H+) |
| C、0.2mol/L NaClO溶液中:c(Na+)=c(HClO)+c(ClO-)+c(OH-) |
| D、0.1mol/L Na2CO3溶液:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com