
【题目】下列物质①NaHSO4 ②HCl ③Cu ④CO2 ⑤Ba(OH)2 ⑥ NaOH ⑦ NaHCO3 ⑧CH3COOH
(1)属于强电解质的是__________(填序号);水溶液能导电的是_______________(填序号)。
(2)写出下列物质在水溶液中的电离方程式
①:__________________________________________
⑦:__________________________________________
⑧:__________________________________________
(3)写出下列物质相互反应的离子方程式
少量的①与⑤:_______________________________________________。
⑥与⑧:_____________________________________________________。
【答案】①②⑤⑥⑦ ①②④⑤⑥⑦⑧ NaHSO4=Na++H++SO42- NaHCO3=Na++HCO3- CH3COOH![]() CH3COO-+H+ H++OH-+Ba2++ SO42-=H2O+BaSO4↓ CH3COOH+H+=CH3COO-+H2O
CH3COO-+H+ H++OH-+Ba2++ SO42-=H2O+BaSO4↓ CH3COOH+H+=CH3COO-+H2O
【解析】
强电解质是在水溶液中或熔融状态下能完全电离的电解质,包括强酸、强碱、活泼金属氧化物和大部分盐;能导电的物质必须含有自由电子或离子,非金属石墨、金属单质和在熔融状态下的电解质或其溶液能导电,据此解答。
①NaHSO4是强酸的酸式盐,是强电解质,其水溶液能导电;
②HCl是强酸,是强电解质,其水溶液能导电;
③Cu是金属单质,能导电,不是电解质也不是非电解质;
④CO2是非电解质,其水溶液能导电;
⑤Ba(OH)2是强碱,是强电解质,其水溶液能导电;
⑥NaOH是强碱,是强电解质,其水溶液能导电;
⑦NaHCO3是盐,是强电解质,其水溶液能导电;
⑧CH3COOH是弱酸,是弱电解质,其水溶液能导电;
(1)根据以上分析可知属于强电解质的是①②⑤⑥⑦;水溶液能导电的是①②④⑤⑥⑦⑧。
(2)NaHSO4是强酸的酸式盐,是强电解质,其电离方程式为NaHSO4=Na++H++SO42-;NaHCO3是弱酸的酸式盐,是强电解质,其电离方程式为NaHCO3=Na++HCO3-;CH3COOH是弱酸,是弱电解质,其电离方程式为CH3COOH![]() CH3COO-+H+。
CH3COO-+H+。
(3)少量的①与⑤反应生成硫酸钡、氢氧化钠和水,离子方程式为H++OH-+Ba2++SO42-=H2O+BaSO4↓。⑥与⑧反应生成醋酸钠和水,离子方程式为CH3COOH+H+=CH3COO-+H2O。


科目:高中化学 来源: 题型:
【题目】下列物质的电离方程式书写正确的是
A. Na2CO3 = Na2+ + CO32
B. NaHCO3 = Na+ + H+ + CO32
C. H2CO3 = 2H+ + CO32
D. Ba(OH)2 = Ba2+ + 2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列物质:①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦ 蔗糖 其中属于电解质的是(填序号)___________,
(2)写出Al2(SO4)3的电离方程式:___________________,
(3)写出NaHSO3(aq) 与稀盐酸反应的离子方程式:_____________________,
(4)胶体是一种常见的分散系,回答下列问题:
①向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为__________________。
②向Fe(OH)3胶体中加入K2SO4饱和溶液,由于SO42-的作用,使胶体形成了沉淀,这个过程叫做胶体的_______。
③区分胶体和溶液常用的方法叫做__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为实验室某浓盐酸试剂瓶上标签的有关内容。取该盐酸10mL,加蒸馏水稀释至250mL,向其中加入mg锌粉恰好完全反应。
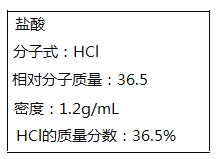
(1)写出锌粉与盐酸反应的离子方程式______________。
(2)求原浓盐酸的物质的量浓度c=____________。
(3)计算出m=___________。
(4)反应中生成的H2可以和标准状况下______mL的O2恰好完全反应。
(5)向反应后的溶液中加入0.6mol/L的AgNO3溶液至不再产生沉淀,共消耗VmL AgNO3溶液,则V的值是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1.5 mol氧气中含有的O2的个数为_____________,标准状况下体积为_________L,与_____________gH2O所含的原子总数相等。
(2)在标准状况下,体积为6.72L的NO和NO2混合气,质量为11.88g,则NO和NO2的体积比为___________。
(3)同温同压下,两种气体A和B的体积之比为2∶1,质量之比为8∶5,则A与B的密度之比为________,摩尔质量之比为_______。
(4)某状况下,2g二氧化碳气体的体积是1120 mL,2gA气体的体积是770 mL,A的摩尔质量是______________。
(5)某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO42-的物质的量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 同分异构体之间分子式相同,其式量也一定相等;式量相等的物质一定是同分异构体
B. 某有机物燃烧后产物只有CO2和H2O,可推出的结论是有机物属于烃
C. 分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可以初步推测有机物结构简式为CH3CH2OH
D. 分子式为C8H10的芳香烃有4种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁可用作燃料的节能消烟剂、抗爆剂等。实验室制备二茂铁装置示意图如图一

已知:①二茂铁熔点是173℃,在100℃时开始升华;沸点是249℃。
②制备二茂铁的反应原理是:2KOH+FeCl2+2C5H6= Fe(C5H5)2+2KCl+2H2O
实验步骤为:
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(C5H6, 密度为0.95g/cm3),搅拌;
③将6.5g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25mL装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入分液漏斗中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的名称是________________________.
(2)步骤①中通入氮气的目的是____________________________________________________.
(3)仪器c的适宜容积应为(选编号):_________
①100mL ②250mL ③500mL
(4)步骤⑤用盐酸洗涤的目的是__________________________________________________
(5)步骤⑦是二茂铁粗产品的提纯,该过程在图二中进行,其操作名称为_________;该操作中棉花的作用是______________________________________________________.
(6)为了确认得到的是二茂铁,还需要进行的一项简单实验是__________________________;若最终制得纯净的二茂铁4.3g,则该实验的产率为____________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述中正确的是
A. 标准状况下,2.24 LCCl4中含有的氯原子数为0.4NA
B. 常温常压下,36g等体积混合的CO与CO2混合气体中含有的氧原子数为1.5NA
C. 1molFe与足量氯气反应时转移的电子数为2NA
D. 1L1mol·L-l的NaClO溶液中含有ClO-的数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com