
【题目】在0.1mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A.加入水时,平衡向逆方向移动
B.加入少量NaOH固体,平衡向正方向移动
C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)不变
D.加入少量CH3COONa固体,平衡向正方向移动
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:

下列说法错误的是:( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X + 3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.改变温度可以改变此反应的平衡常数
D.增大压强使平衡向生成Z的方向移动,平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示。下列有关叙述正确的是
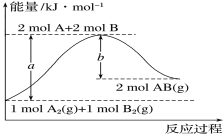
A.每生成2molAB(g)吸收bkJ热量
B.断裂1molA—A键和1molB—B键,放出akJ能量
C.该反应中反应物的总能量高于生成物的总能量
D.反应热ΔH=+(a-b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把活泼金属片a和b放在盛有稀食盐水和酚酞混合液的表面皿中,构成如图所示原电池,一段时间后观察到区域I变红色,则下列叙述正确的是( )
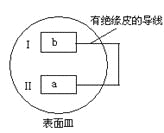
A.a是原电池的负极B.b的活泼性大于a
C.无电流产生D.b 电极上有气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:

mA(s)+nB(g)![]() pC(g)+qD(g)。达到平衡后,测得B的浓度为0.5mol/L。保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后,测得B的浓度为0.2mol/L,当其它条件不变时,C在反应混合物中的体积分数(x)与温度(T)、时间(t)的关系如图所示,下列叙述正确的是
pC(g)+qD(g)。达到平衡后,测得B的浓度为0.5mol/L。保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后,测得B的浓度为0.2mol/L,当其它条件不变时,C在反应混合物中的体积分数(x)与温度(T)、时间(t)的关系如图所示,下列叙述正确的是
A. 容积扩大到原来的两倍,平衡向逆反应方向移动
B. 化学方程式中n>p+q
C. 达到平衡后,若升高温度,平衡向逆反应方向移动
D. 达到平衡后,增加A的量,有利于提高B的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原SiHCl3(沸点:31.85℃)制备纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是( )

A. 装置Ⅱ、Ⅲ中依次盛装的是浓H2SO4、冰水
B. 实验时,应先加热管式炉,再打开盛装稀硫酸的分液漏斗
C. 为鉴定制得的硅中是否含微量铁单质,需要用到的试剂为盐酸、双氧水、硫氰化钾溶液
D. 该实验中制备氢气的装置也可用于氧氧化钠稀溶液与氯化铵固体反应制备氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)可逆反应2SO2(g)+O2(g)![]() 2SO3(g);ΔH<0,在其他条件不变时,
2SO3(g);ΔH<0,在其他条件不变时,
①升温反应速率________,增大压强反应速率________;
②达到化学平衡时,v正(SO2)________(填“大于”“小于”或“等于”)v逆(SO3);若平衡后增加O2的浓度,平衡向________方向移动,SO2的转化率________;若升高温度,则平衡向________方向移动。
(2)将等物质的量的A、B、C、D四种物质混合,发生如下反应:aA+bB![]() cC(s)+dD,当反应进行一定时间后,测得A减少了nmol,B减少了
cC(s)+dD,当反应进行一定时间后,测得A减少了nmol,B减少了![]() nmol,C增加了
nmol,C增加了![]() nmol,D增加了nmol,此时达到化学平衡,该化学方程式中各物质的系数为:a=______、b=______、c=______、d=______。
nmol,D增加了nmol,此时达到化学平衡,该化学方程式中各物质的系数为:a=______、b=______、c=______、d=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.40gNaOH中含有的共用电子对数为2NA
B.常温常压下,1.8g甲基(—CD3)中含有的中子数为0.9NA
C.31g白磷(![]() )含有共价键的总数为6NA
)含有共价键的总数为6NA
D.标况下,22.4LH2O中所含氢氧键的数目约为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com