
【题目】汽车尾气中的NO(g) 是导致光化学烟雾和破坏臭氧层的重要源头之一。现拟用下列方法处理NO,根据题意回答下列问题:
(1)采用某种催化剂催化分解NO,发生反应2NO(g)![]() N2(g)+O2(g),在T1℃ 和T2℃时(T1>T2)NO的转化率随时间变化的结果如图所示。
N2(g)+O2(g),在T1℃ 和T2℃时(T1>T2)NO的转化率随时间变化的结果如图所示。
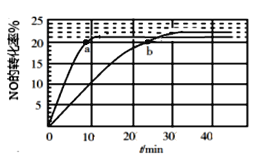
① 反应 2NO(g)![]() N2(g)+O2(g) 为(填“吸热”或“放热”)____________反应。
N2(g)+O2(g) 为(填“吸热”或“放热”)____________反应。
② T2℃时,反应的平衡常数K=__________(保留2位小数)。
③ 在T1℃下,要提高NO转化率,可采取的措施是_________________________
④ 比较a、b处反应速率大小:va(正)________ vb(逆)(填“大于”“小于”或“等于”)。已知反应速率 v正=k正x2(NO),v逆=k逆 x(N2)·x(O2),k正、k逆 分别为正、逆向反应速率常数,x为物质的量分数,计算b点处v(正)/v(逆)=__________(保留1位小数)。
(2)臭氧也可用于处理NO.O3氧化NO结合水洗可产生HNO3和O2,写出该反应的化学方程式___________________,每生成1mol的HNO3转移_______mol电子.
【答案】放热 0.02 移走生成物 大于 1.3 3O3+2NO+H2O═2HNO3+3O2 3
【解析】
(1) ①根据图像分析,温度越高,化学反应速率越快,越先达到平衡,从图像看出温度高时NO转化率低,所以反应 2NO(g)![]() N2(g)+O2(g)为放热反应;
N2(g)+O2(g)为放热反应;
② T2℃时,根据图像可以知道NO的平衡转化率为22%,三行式法计算平衡常数;
③温度一定时,可减少生成物浓度,平衡正向移动,提高转化率;压强对此反应无影响;
④温度越高,化学反应速率越快,比较a、b处反应速率大小;根据平衡常数计算 k正、k逆的关系,再根据b点计算v(正)/v(逆);
(2)O3氧化NO结合水洗可产生HNO3和O2,写出化学方程式;O3氧化NO结合水洗可产生HNO3和O2,转移电子数=化合价升高数,NO转化为HNO3 ,化合价升高3,每生成1mol的HNO3转移3mol电子。
(1) ①根据图像分析,温度越高,化学反应速率越快,越先达到平衡,从图像看出温度高时NO转化率低,所以反应 2NO(g)![]() N2(g)+O2(g)为放热反应;
N2(g)+O2(g)为放热反应;
正确答案:放热反应。
② T2℃时,根据图像可以知道NO的平衡转化率为22%,三行式法计算平衡常数;
2NO(g)![]() N2(g)+O2(g)
N2(g)+O2(g)
C(初) 1 0 0
△C 0.22 0.11 0.11
C(末) 0.78 0.11 0.11
K=![]() ≈0.02;
≈0.02;
正确答案:0.02。
③温度一定时,可减少生成物浓度,平衡正向移动,提高转化率;压强对此反应无影响;
正确答案:移走生成物。
④温度越高,化学反应速率越快,所以va(正)大于vb(逆);根据平衡常数计算 k正、k逆的关系,再根据b点计算v(正)/v(逆);
T2℃时,平衡时v(正)= v(逆), 即k正x2(NO)平衡 =k逆 x(N2)平衡·x(O2)平衡,得k (正)/ k (逆)= x(N2)平衡·x(O2)平衡/ x2(NO)平衡=K=0.02(提示:前面计算所得);
b点时NO转化率为20%,列三行式
2NO(g)![]() N2(g)+O2(g)
N2(g)+O2(g)
C(初) 1 0 0
△C 0.20 0.10 0.10
C(末) 0.80 0.10 0.10
b点处v(正)/v(逆)= k正x2(NO)/ (k逆 x(N2)·x(O2))=![]() ×
×![]() =0.02×64=1.3
=0.02×64=1.3
正确答案: 大于 1.3。
(2) O3氧化NO结合水洗可产生HNO3和O2,写出化学方程式3O3+2NO+H2O═2HNO3+3O2;O3氧化NO结合水洗可产生HNO3和O2,转移电子数=化合价升高数,NO转化为HNO3 ,化合价升高3,每生成1mol的HNO3转移3mol电子。
正确答案:3O3+2NO+H2O═2HNO3+3O2 3。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72LH2(已折算成标准状况),甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25g/L。请回答下列问题:
(1)甲的化学式是__________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________。
(3)气体丙与金属镁反应的产物是__________(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式__________。有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之__________(已知Cu2O+2H+=Cu+Cu2++H2O)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5 表示。有关说法正确的是

A. 该装置为原电池,b为原电池的负极
B. 中间室Na+移向右室,Cl-移向左室,a极区溶液的pH减小
C. 当左室有4.48L(标准状况下)CO2生成时,右室产生的N2为0.8mol
D. b电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将8 mL NO2和O2的混合气体通入倒立于水槽中装满水的量筒,充分反应后,剩余气体为1 mL,则原混合气体中NO2和O2的体积比可能为 ( )
A. 7∶5 B. 3∶7 C. 7∶1 D. 1∶7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向1L 0.1mol/L的一元酸HR溶液中逐渐通入氨气(已知25℃时一水合氨的电离平衡常数为K=1.76×10-5),保持溶液的温度和体积不变,混合溶液的pH与粒子浓度比值的对数变化关系如图所示。下列叙述错误的是
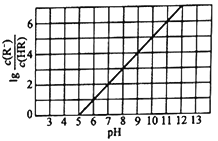
A. 25℃时,0.1mol/L的一元酸HR的电离平衡常数为Ka=10-5
B. 当通入0.1mol氨气时,c(NH4+)>c(R-)>c(OH-)>c(H+)
C. 当c(R-)=c(HR) 时,溶液为酸性
D. HR为弱酸,25℃时随着氨气的通入,c (R-)/[c(OH)c (HR)] 逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
(1)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式__________。
(2)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)![]() SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol1
SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol1
3SiH2Cl2(g)![]() SiH4(g)+2SiHCl3 (g) ΔH2=30 kJ·mol1
SiH4(g)+2SiHCl3 (g) ΔH2=30 kJ·mol1
则反应4SiHCl3(g)![]() SiH4(g)+ 3SiCl4(g)的ΔH=__________ kJ·mol1。
SiH4(g)+ 3SiCl4(g)的ΔH=__________ kJ·mol1。
(3)对于反应2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
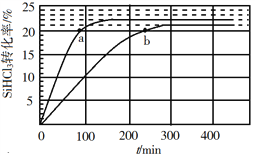
①343 K时反应的平衡转化率α=_________%。平衡常数K343 K=__________(保留2位小数)。
②在343 K下:要提高SiHCl3转化率,可采取的措施是___________;要缩短反应达到平衡的时间,可采取的措施有____________、___________。
③比较a、b处反应速率大小:υa________υb(填“大于”“小于”或“等于”)。反应速率υ=υ正υ逆=![]()
![]() ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处![]() =__________(保留1位小数)。
=__________(保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍。下列说法正确的是
A.简单阳离子的氧化性:![]()
B.气态氢化物的沸点:![]()
C.X、Z与M不可能存在同一离子化合物中
D.Y2Z的溶液:c(Y+):c(Z2-) > 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相同物质的量浓度下的各溶液:NaX、NaY、NaZ,其pH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序为:________________________________
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是__________________
(3)在一定温度下,有a盐酸,b硫酸,c醋酸三种酸。(填序号)
①当其物质的量浓度相同时,c(H+)由大到小的顺序是 _______________。
②同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是 ____________。
③当三者c(H+)相同时,物质的量浓度由大到小的顺序为 ____________________。
(4)难溶电解质的水溶液中存在着溶解平衡。已知:在常温下, K sp [Cu(OH)2]=2.0×10-20写出Cu(OH)2溶度积常数表达式___________________________________当溶液中各离子浓度系数次方的乘积大于溶度积时,则产生沉淀,反之沉淀溶解。某CuSO4溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于 _______________才能达到目的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液中离子关系的说法正确的是( )
A. 0.1 mol·L-1NaHCO3溶液中离子浓度关系:c(Na+)=2c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
B. 把0.2 mol/L NH4Cl溶液与0.1 mol/L NaOH溶液等体积混合后离子浓度关系:c(Cl-)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
C. 常温,向醋酸钠溶液中滴加少量醋酸使其pH=7,则混合液中:c(Na+)=c(CH3COO-)
D. 在Na2CO3溶液中,c(H+)+c(![]() )+c(H2CO3)= c(OH-)
)+c(H2CO3)= c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com