
【题目】沉淀的生成、溶解和转化在无机物制备和提纯以及科研等领域有广泛应用。
Ⅰ.汽车尾气中的SO2可用石灰水来吸收,生成CaSO3浊液。已知常温下Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9 常温下测得某纯CaSO3与水形成的浊液pH=9,忽略SO32-的第二步水解,则Ksp(CaSO3)=__________ 。CaSO3易变质为CaSO4,水垢中含有较多的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。CaSO4转化为CaCO3的离子方程式为:_________;
Ⅱ.已知25℃时,NH3H2O电离常数Kb=1.8×10-5,Ksp[Mg(OH)2]=1.0×10-11,向0.4mol/L的氨水中加入等体积浓度为6×10-4mol/L MgCl2 溶液,________沉淀生成(填“无”或“有”),并简述理由______;若某溶液中C(Mg2+)=1.2×10-3mol/L,需向其中加入等体积的NaOH溶液浓度为_____ mol/L时,可使Mg2+恰好沉淀完全(忽略溶液体积变化)。
Ⅲ.工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有还原沉淀法,该法的工艺流程为:
CrO42-![]() Cr2O72-
Cr2O72-![]() Cr3+
Cr3+![]() Cr(OH)3
Cr(OH)3
其中第①步存在平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
①若平衡体系的pH=2,则溶液显____________色。
②能说明第①步反应达平衡状态的是_____________。
A.Cr2O72-和CrO42-的浓度相同 B.2v (Cr2O72-) =v (CrO42-) C.溶液的颜色不变
③第②步中,还原1mol Cr2O72-离子,需要________mol的FeSO4·7H2O。
④第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+ (aq)+3OH-(aq) 常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至__________。
Cr3+ (aq)+3OH-(aq) 常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至__________。
【答案】 4.2×10-9 CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq) 有 因为C(OH-)=(KbC)1/2,Qc=C(Mg2+)C(OH-)2=1.08×10-9>Ksp 4.4×10-3 橙 c 6 5
CaCO3(s)+SO42-(aq) 有 因为C(OH-)=(KbC)1/2,Qc=C(Mg2+)C(OH-)2=1.08×10-9>Ksp 4.4×10-3 橙 c 6 5
【解析】Ⅰ由Ka2(H2SO3)=6.0×10-9可知SO32-+H2O![]() HSO3-+OH-的水解平衡常数
HSO3-+OH-的水解平衡常数![]() 。常温下,测得某纯CaSO3与水形成的浊液pH为9,忽略第二步水解可以得到:c(HSO3-)=c(OH-)=1×10-5mol/L,可知
。常温下,测得某纯CaSO3与水形成的浊液pH为9,忽略第二步水解可以得到:c(HSO3-)=c(OH-)=1×10-5mol/L,可知 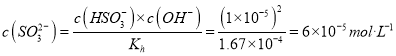 。又c(Ca2+)=c(SO32-)+c(HSO3-)=7×10-5 mol/L,所以Ksp(CaSO3)=c(Ca2+)×c(SO32-)=7×10-5×6×10-5=4.2×10-9。碳酸钙比硫酸钙更难溶,可以通过增大碳酸根浓度的方法将硫酸钙转化为碳酸钙,反应为:CaSO4(s)+CO
。又c(Ca2+)=c(SO32-)+c(HSO3-)=7×10-5 mol/L,所以Ksp(CaSO3)=c(Ca2+)×c(SO32-)=7×10-5×6×10-5=4.2×10-9。碳酸钙比硫酸钙更难溶,可以通过增大碳酸根浓度的方法将硫酸钙转化为碳酸钙,反应为:CaSO4(s)+CO![]() (aq)
(aq)![]() CaCO3(s)+SO
CaCO3(s)+SO![]() (aq)。
(aq)。
Ⅱ、氨水存在电离平衡:NH3·H2O![]() NH4+ + OH,忽略水电离,认为铵根离子浓度等于氢氧根离子浓度,考虑电离的氨水很少,所以NH3·H2O的浓度近似就是0.2mol/L(注意溶液体积是原来2倍,各自浓度都是一半)。根据平衡常数可以计算c(OH-)=
NH4+ + OH,忽略水电离,认为铵根离子浓度等于氢氧根离子浓度,考虑电离的氨水很少,所以NH3·H2O的浓度近似就是0.2mol/L(注意溶液体积是原来2倍,各自浓度都是一半)。根据平衡常数可以计算c(OH-)=![]() 。c(Mg2+)=3×10-4mol/L,所以Qc=3×10-4×
。c(Mg2+)=3×10-4mol/L,所以Qc=3×10-4×![]() =1.08×10-9>Ksp,所以有沉淀。
=1.08×10-9>Ksp,所以有沉淀。
Ⅲ:①若平衡体系的pH=2,在酸性环境下,化学反应平衡正向移动,溶液显示橙色。
②a.Cr2O72-和CrO42-的浓度相同,没有强调不变,所以不一定平衡,故a错误;b.式中未说明反应速率是指正反应还是逆反应,无法判断是不是平衡状态,故b错误;c.溶液的颜色不变,证明各组分的浓度不随时间的变化而变化,故c正确。
③第②步中,还原1molCr2O72-离子,即得到了6mol的电子,根据氧化还原反应中的电子守恒,硫酸亚铁中的亚铁离子变为三价铁离子失去1个电子,所以需要6mol的FeSO4·7H2O。
④c(Cr3+)降至10-5mol/L, ![]() ,所以pH=5。
,所以pH=5。


科目:高中化学 来源: 题型:
【题目】已知乙酸乙酯(C4H8O2)是一种无色液体,不溶于水,密度小于1 g·mL-1,沸点约为55 ℃。要从水与乙酸乙酯的混合物中将乙酸乙酯分离出来,下列方法中最简便的是
A.蒸馏B.分液C.过滤D.蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为某反应的微观模拟示意图。

(1)图中的氧化物有________种。
(2)该反应的化学方程式为_________________________,属于_____________(填基本反应类型)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理对生产有重大的指导意义。回答下列问题:
(1)有两个温度相同的密闭容器A和B,容器A保持容积不变,容器B保持压强不变,起始时向容积相等的A、B中分别充入等量的C(碳)和H2O(g),发生反应:C(s)+H2O(g)![]() CO(g)+ H2(g) (正反应为吸热反应),并分别达到平衡。
CO(g)+ H2(g) (正反应为吸热反应),并分别达到平衡。
①H2O的体积分数:V(A)%_____V(B)%。(填“>”、“<” “=”)
②达到平衡后,在两容器中分别通入等量的氦气,则A中H2O的转化率_______(填“增大” “减小”、“不变”);B中化学平衡_________移动(填“不”“向正反应方向”“向逆反应方向”)。
(2)某温度下,测得0.01mol·L-1 NaOH溶液的pH=10,则在该温度下Kw=______;在此温度下,将pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合,若所得溶液为中性,则a:b=_______(假设混合时体积不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人尿中可以分离出具有生长素效应的化学物质——吲哚乙酸,吲哚乙酸的结构如下图所示。
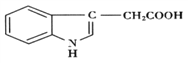
下列有关说法正确的是
A. 吲哚乙酸与苯丙氢酸互为同系物
B. 吲哚乙酸苯环上的二氯代物共有四种
C. 1mol吲哚乙酸与足量氢气发生反应,最多消耗5molH2
D. 吲哚乙酸可以发生取代反应、氧化反应和还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为某化工企业生产流程示意图,下列说法正确的是( )

A. 钛酸亚铁(FeTiO3)中钛元素为+3价
B. ①中反应为:2FeTiO3+6C+7Cl2==== 2X+2TiCl4+6CO,则X为FeCl3
C. ③中氩气(Ar)作反应物,反应类型为置换反应
D. ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图一所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液,足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。

(1)图一中的直流电源为一种性能优良的Al-Ag2O电池,其原理如图二所示。该电池中铝是负极,试写出电池工作时的正极反应式__________________和电池的总化学反应方程式______________。
(2)接通电源后,经过一段时间后,测得丙中K2SO4质量分数为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为_______极;c电极上发生______反应(“氧化”或“还原”);
②电极b上发生的电极反应为___________________;
③列式计算电极b上生产的气体在标准状况下的体积_______;
④电极c的质量变化是_____g;
⑤电解前后各溶液的pH是否发生变化(“增大”、“减小”或“不变”)
甲溶液_________;乙溶液_________;丙溶液______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3②NO2进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度为( )

A. ①>② B. ①<② C. ①=② D. 不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com