
下列反应最终能生成Fe3+的化合物的是()
①过量Fe与HNO3
②铁丝在硫蒸汽中燃烧
③向FeBr2溶液中通入Cl2
④铁与CuCl2溶液反应
⑤Fe(OH)2露置于空气中.
A. ①②③ B. ①③⑤ C. ③④ D. ③⑤
考点: 铁盐和亚铁盐的相互转变.
分析: ①Fe与HNO3反应生成硝酸铁,Fe3+与Fe反应生成Fe2+;
②铁丝在硫蒸汽中燃烧生成FeS;
③向FeBr2溶液中通入Cl2,Fe2+还原性大于Br﹣,氯气首先把Fe2+氧化为Fe3+;
④铁与CuCl2溶液反应生成氯化亚铁和铜;
⑤Fe(OH)2露置于空气中,与氧气、水反应生成氢氧化铁.
解答: 解:①Fe与HNO3反应生成硝酸铁,Fe3+与Fe反应生成Fe2+,故不选;
②铁丝在硫蒸汽中燃烧生成FeS,故不选;
③向FeBr2溶液中通入Cl2,Fe2+还原性大于Br﹣,氯气首先把Fe2+氧化为Fe3+,故选;
④铁与CuCl2溶液反应生成氯化亚铁和铜,故不选;
⑤Fe(OH)2露置于空气中,与氧气、水反应生成氢氧化铁,故选;
故选D.
点评: 本题考查了铁及其化合物的性质,难度不大,掌握元素及其化合物的性质是解题的关键,注意氧化剂氧化还原剂时的先后顺序.


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
据实验证明:用漂白粉溶液浸泡过的有色布条,如果晾置在空气中,过了一段时间,其漂白效果会更好,原因可能是()
A. 漂白粉被氧化了
B. 有色布条被空气中的氧气氧化了
C. 漂白粉溶液跟空气中的CO2反应充分,生成了较多量的HClO
D. 漂白粉溶液蒸发掉部分水,其浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
将Fe(OH)3胶体与BaCl2的混合液装在半透膜中,浸泡在装有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜有破损的是()
A. 溶液为黄色
B. 能产生丁达尔效应
C. 加入AgNO3 溶液产生白色沉淀
D. 加入Na2SO4 溶液产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
由A、B两种粉末组成的混合物,在一定条件能发生如图所示的转化关系.其中B、C均为氧化物,J为黄绿色气体,部分反应产物已略去.
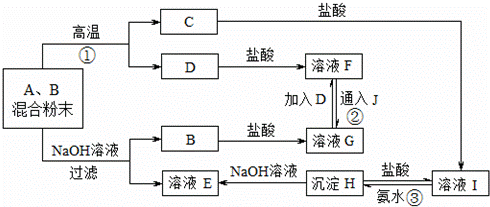
请 回答:
回答:
(1)写出相应物质的化学式:A ,B
(2)写出图中相应转化的离子方程式:反应② 反应③ (3)反应①的主要用途是 (回答一条即可).
(4)以下选项中的试剂可以检验溶液F中的金属阳离子的是 (填字母编号).
a.NaOH溶液 b.KSCN溶液 c.稀硫酸 d.新制氯水与KSCN溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列说法中不正确的是()
A. 一定量的Fe与含1molHNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA
B. 1molFeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
C. 0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA
D. 125gCuSO4•5H2O晶体中含有0.5NA个Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验基本操作或说法正确的是 (填写序号)
A、用50ml的量筒量取5.2ml稀硫酸
B、为了有效地除去粗盐中的Ca2+、Mg2+、SO42﹣,可先加入NaOH,再加入BaCl2,最后加入Na2CO3,将沉淀过滤后,再用HCl调整溶液至中性
C、石蕊试纸或PH试纸使用前都应用蒸馏水润湿
D、稀释浓硫酸时,应将水沿器壁缓缓加入浓硫酸中,并不断用玻璃棒搅拌
E、容量瓶中含有少量蒸馏水,对配制一定物质的量浓度的硫酸溶液无影响
F、将饱和FeC13溶液滴加沸水中,然后继续加热并不断搅拌可制得氢氧化铁胶体;
G、乙酸乙酯制备收集完毕,分液时,直接将乙酸乙酯从分液漏斗的上口倒出
H、在粗盐的提纯实验中,溶解、过滤、蒸发都用到了玻璃棒.
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组探究SO2气体还原Fe,I2,他们使用的药品和装置如如所示.
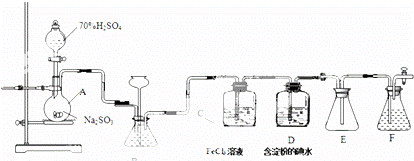
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若 ,则整个装置气密性良好.装置E的作用是 .装置F中为NaOH溶液.
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 .
a.蒸馏水
b.饱和Na2SO3溶液
c.饱和NaHSO3溶液
d.饱和NaHCO3溶液
(3)SO2气体还原Fe3+反应的产物是 (填离子符号).
(4)在上述装置中通入过量的SO2为了验证C中SO2与Fe3+发生了氧化还原反应,他们取C中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去.
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀.
上述方案不合理的是方案①,原因是 .
(5)能表明I﹣的还原性弱于SO2的现象是 ,写出有关离子方程式: ﹣.
查看答案和解析>>
科目:高中化学 来源: 题型:
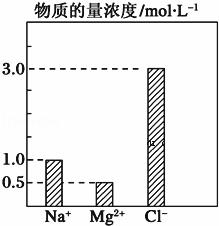
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
(1)该混合液中含溶质MgCl2的物质的量为 ,
(2)将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 1mol C10H22含共价键数目32NA
B. 常温常压下,8g CH4含有电子数目5NA
C. 1L 0.1mol•L﹣1的醋酸溶液中含有CH3COO﹣的数目0.1NA
D. 78g苯含有C=C双键的数目为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com