
|
0.1 mol/L Na2SO4溶液300 mL、0.1 mol/L MgSO4溶液200 mL和0.1 mol/L Al2(SO4)3溶液100 mL,这三种溶液中硫酸根离子浓度之比是 | |
| [ ] | |
A. |
1∶1∶1 |
B. |
3∶2∶1 |
C. |
3∶2∶3 |
D. |
1∶1∶3 |
科目:高中化学 来源:山东省曲阜一中2010-2011学年高二下学期期末考试化学试题 题型:013
|
设NA表示阿伏加德罗常数值,下列叙述正确的是 | |
| [ ] | |
A. |
NA个氧气分子和NA个氢气分子的质量比为16∶1 |
B. |
标准状况下, 22.4 L H2O含有的分子数为NA |
C. |
11.2 L氯气中含有的原子数为NA个 |
D. |
2 L 1 mol/L Na2SO4溶液中Na+离子数为2NA个 |
查看答案和解析>>
科目:高中化学 来源:广东省东莞市光明、常平、厚街、万江四校2010-2011学年高一上学期期中联考化学试题 题型:021
|
下列溶液中,跟200 ml 0.5 mol/L Na2CO3溶液所含Na+的物质的量浓度相同的是 | |
A. |
400 ml 0.25 mol/L NaCl溶液 |
B. |
200 ml 1 mol/L NaCl溶液 |
C. |
100 ml 0.5 mol/L Na2SO4溶液 |
D. |
100 ml 2 mol/L NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高二版(选修4) 2009-2010学年 第11期 总第167期 人教课标版(选修4) 题型:022
常温下,将
0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合后(忽略混合后溶液体积的变化),测得混合溶液的pH等于8.试回答下列问题:(1)混合溶液的pH等于8的原因是(用离子方程式表示)________.
(2)混合溶液中由水电离出的c(H+)________0.1 mol/L NaOH溶液中由水电离出的c(H+)(填“大于”、“小于”或者“等于”).
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+)-c(A-)=________mol/L;
c(OH-)-c(HA)=________mol/L.
查看答案和解析>>
科目:高中化学 来源:黑龙江省大庆铁人中学2011届高三上学期期末考试化学试题 题型:022
草酸(H2C2O4)是一种易溶于水的二元中强酸,在水中它的存在形态有H2C2O4、HC2O![]() 、C2O
、C2O![]() ,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:
,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:
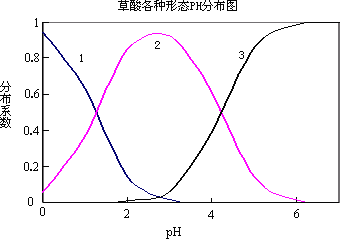
(1)图中曲线1表示________的分布系数变化;曲线3表示________的分布系数变化.
现有物质的量浓度均为0.1 mol/L的下列溶液:
①Na2C2O4
②NaHC2O4
③H2C2O4
④(NH4)2C2O4
⑤NH4HC2O4
已知NaHC2O4溶液显酸性.
(2)Na2C2O4溶液中,c(Na+)/c(C2O![]() )________2(填“>”、“=”、“<”),原因是________(用离子方程式表示).
)________2(填“>”、“=”、“<”),原因是________(用离子方程式表示).
(3)常温下,向10 mL 0.1 mol/L H2C2O4溶液中滴加0.1 mol/L NaOH溶液,随着NaOH溶液体积的增加,当溶液中c(Na+)=2c(C2O![]() )+c(HC2O
)+c(HC2O![]() )时,溶液显________性(填“酸”、“碱”或“中”),且V(NaOH)________10 mL(填“>”、“=”或“<”).
)时,溶液显________性(填“酸”、“碱”或“中”),且V(NaOH)________10 mL(填“>”、“=”或“<”).
(4)下列关于五种溶液的说法中,正确的是
A.
溶液②中,c(C2OB.
溶液②中,c(H2C2O4)+c(OH-)=c(C2OC.溶液④⑤中都符合c(NH![]() )+c(H+)=c(HC2O
)+c(H+)=c(HC2O![]() )+2c(C2O
)+2c(C2O![]() )+c(OH-)
)+c(OH-)
D.五种溶液都符合c(H2C2O4)+c(HC2O![]() )+c(C2O
)+c(C2O![]() )=0.1 mol·L-1.
)=0.1 mol·L-1.
(5)五种溶液中c(H2C2O4)
由大到小排列的顺序是________.(6)
配平氧化还原反应方程式:![]()
(7)
称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液.量取两份此溶液各25 mL,分别置于两个锥形瓶中.第一份溶液中加入2滴酚酞试液,滴加0.25 mol/L NaOH溶液至20 mL时,溶液由无色变为浅红色.第二份溶液用0.10 mol/L酸性KMnO4溶液滴定,滴定终点如何判断________.当加入16 mL 0.10 mol/L酸性KMnO4溶液时恰好反应完全.则原试样中H2C2O4·2H2O的质量分数为________,KHC2O4的质量分数为________.如果用0.25 mol/L NaOH溶液滴定第一份溶液的实验滴定终点仰视读数则测得的KHC2O4的质量分数________(填“偏高”“偏低”或“无影响”)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com