
| 鉴别物 | 试剂 | 现象 | 化学方程式 |
| 乙醛与己烯 | |||
| 甲醇与乙醚 | |||
| 福尔马林与丙醇 | |||
| 乙烷与乙烯 |
| △ |
| 水浴 |
| 鉴别物 | 试剂 | 现象 | 化学方程式 | ||
| 乙醛 己烯 | 新制氢氧化铜 | 有红色沉淀生成的是乙醛 | CH3CHO+2Cu(OH)2
| ||
| 甲醇 乙醚 | 金属钠 | 有气体生成者是甲醇 | 2CH3OH+2Na→CH3ONa+H2↑ | ||
| 福尔马林丙醇 | 银氨溶液 | 试管内壁有银白色物质附着的是福尔马林 | HCHO+4Ag(NH3)2OH
| ||
| 乙烷 乙烯 | 溴水 | 能够使溴水褪色的是乙烯 | CH2=CH2+Br2→CH2BrCH2Br |


科目:高中化学 来源: 题型:
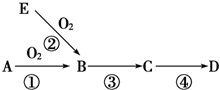 已知A是一种常见非金属单质,B是氧化物,E是A的氢化物,D是A的最高价氧化物对应的水化物,其转化关系如图所示:
已知A是一种常见非金属单质,B是氧化物,E是A的氢化物,D是A的最高价氧化物对应的水化物,其转化关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定溶质质量分数溶液的配制 |
| B、用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验 |
| C、用普通漏斗组成的过滤装置进行过滤实验 |
| D、将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com