
下列与有机物的结构、性质有关的叙述正确的是
A.用新制氢氧化铜悬浊液无法鉴别葡萄糖和乙酸
B.乙酸与乙醇可以发生酯化反应,又均可与碳酸氢钠溶液反应
C.硫酸铵、硫酸铜和乙醇均能使蛋白质变性
D.二氯甲烷不存在同分异构体
科目:高中化学 来源:2013-2014辽宁省大连市高三双基测试化学试卷(解析版) 题型:简答题
(15分)(1)25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。请回答下列问题:
①HA是________(填“强电解质”或“弱电解质”);
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是________(填字母)。
A.c(H+)/c(HA) B.c(HA)/(A-) C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是 (用序号连接)
(3)若1mol SO2(g)氧化为1mol SO3(g)的ΔH =-99kJ·mol-1,单质硫的燃烧热为296kJ·mol-1,则由S(s)生成3 mol SO3(g)的ΔH =
(4)对于2NO2(g) N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。

①.A、C两点的反应速率:A>C
②.A、C两点气体的颜色:A深、C浅
③.B、C两点的气体的平均分子质量:B<C
④.由状态B到状态A,可以用加热方法
(5)下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图:
请回答:
① 甲烷燃料电池的负极反应式是 。
② 当线路中有0.2 mol电子通过时,阴极增重____g。
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省五校第二学期期末联考高一化学试卷(解析版) 题型:选择题
A、B分别为同一主族第三周期、第四周期的不同元素的原子,它们原子核内质子数均等于中子数。若A为ⅡA 族,其质量数为x,则B的质子数为Z;若A为ⅣA族,其质子数为y,则B的质量数为N。Z和N为下列哪一组值
A.Z: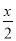 +18,N:2y+18 B.Z:
+18,N:2y+18 B.Z: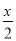 +8, N:2y+18
+8, N:2y+18
C.Z: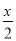 +8, N:2y+36 D.Z:
+8, N:2y+36 D.Z: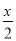 +18, N:2y+36
+18, N:2y+36
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省五校第二学期期末联考高一化学试卷(解析版) 题型:选择题
下列说法中正确的一组是
A.H2和D2互为同素异形体;
B. 和
和 互为同分异构体;
互为同分异构体;
C.正丁烷和异丁烷是同系物;
D. 和
和 是同一种物质
是同一种物质
查看答案和解析>>
科目:高中化学 来源:2013-2014福建龙岩市毕业联合考试理综化学试卷(解析版) 题型:选择题
对于反应aA+bB=dD+eE,该化学反应速率定义为 。式中
。式中 指物质
指物质 的反应速率,
的反应速率, 、
、 、
、 、
、 是化学计量数。298k时,测得溶液中的反应H2O2+2HI=2H2O+I2在不同浓度时化学反应速率v见下表:
是化学计量数。298k时,测得溶液中的反应H2O2+2HI=2H2O+I2在不同浓度时化学反应速率v见下表:
实验编号 | 1 | 2 | 3 | 4 |
c(HI)/ mol·L-1 | 0.100 | 0.200 | 0.300 | 0.100 |
c(H2O2)/ mol·L-1 | 0.100 | 0.100 | 0.100 | 0.200 |
v/ mol·L-1·s-1 | 0.00760 | 0.0153 | 0.0227 | 0.0151 |
以下说法正确的是
A.实验1、2中, (H2O2)相等
(H2O2)相等
B.将浓度均为0.200 mol·L-1H2O2和HI溶液等体积混合,反应开始时 =0.0304 mol·L-1·s-1
=0.0304 mol·L-1·s-1
C. 与“HI和H2O2浓度的乘积”的比值为常数
与“HI和H2O2浓度的乘积”的比值为常数
D.实验4,反应5秒后H2O2浓度减少了0.0755 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三高考模拟理综化学试卷(解析版) 题型:简答题
雾霾天气严重影响人们的生活质量,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法。
(1)氮、氧元素非金属性较强的是 。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:
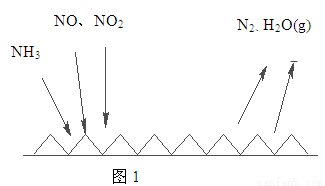
①由图1可知SCR技术中的氧化剂为 。
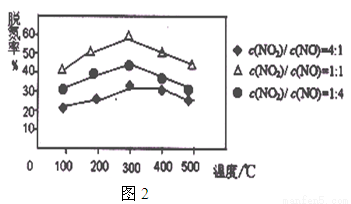
②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)= 。当NO2与NO的物质的量之比为1:1时,用氨脱氮,每生成1molN2放出的热量为QkJ,写出该反应的热化学方程式 。
(3)海水具有良好的吸收SO2的能力,其吸收过程如下:
①SO2溶于海水生成H2SO3,H2SO3最终会电离出SO32-,SO32-可以被海水中的溶解氧氧化为SO42-。海水的pH会 (填“升高” 、“不变”或“降低”)。
②SO2和O2在H2SO4溶液中可以构成原电池,其负极反应式是 。
(4)碲(Te)为ⅥA族元素,是当今高新技术新材料的主要成分之一。工业上可将SO2通入TeCl4的酸性溶液中进行“还原”得到碲,该反应的化学方程式是_________ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:推断题
(13分)(1).PET是应用广泛的五大工程塑料之一,PET结构片段:
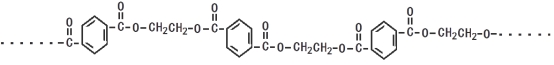
①PET由两种有机物通过缩聚反应生成,其中分子较大的单体分子结构简式为 ,分子较小的单体含氧官能团名称是 。
②PET塑料有多种降解途径,其中常用的甲醇法是在一定条件下将其与过量的甲醇作用,降解为两种小分子。该反应的化学方程式为: 。
(2).水杨酸(邻羟基苯甲酸)是合成阿司匹林(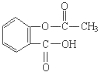 )的原料。
)的原料。
①水杨酸与乙酸酐(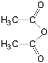 )反应生成阿司匹林的化学方程式: 。
)反应生成阿司匹林的化学方程式: 。
②写出一种阿司匹林同分异构体的结构式 ,该同分异构体符合以下条件:
a.芳香族化合物;
b.与氢氧化钠溶液共热,完全反应将消耗四倍物质的量的氢氧化钠;
c.苯环上氢原子被一个溴原子取代,可能的产物有两种。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
短周期元素X、Y、W、Q在元素周期表中的相对位置如下图所示。Y是地壳中含量最多的元素。下列说法正确的是( )
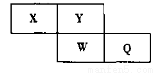
A.1mol Q单质与氢氧化钠溶液反应转移的电子数目为2 NA
B.X的气态氢化物能使湿润的蓝色石蕊试纸变红
C.氢化物的沸点:H2Y>HQ
D.最髙价氧化物的水化物的酸性:W > Q
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:选择题
已知在2L密闭容器内,发生:2NO(g)+O2(g)?2 NO 2(g),不能说明该反应已达到平衡状态的是( )
A.容器内颜色保持不变 B.v逆(NO)=2v正(O2)
C.单位时间内生成amol的O2,同时生成2amolNO2 D.容器内密度保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com