
某温度时,浓度均为1 mol·L-1的两种气体X2、Y2,在容积不变的密闭容器中发生反应,反应结束时,容器内各物质的浓度为:c(X2)=0.6 mol·L-1,c(Y2)=1.2 mol·L-1,c(Z)=0.4 mol·L-1。则该反应的化学方程式为( )
A.2X2+Y2====2Z B.X2+Y2====2Z
C.2X2![]() Y2+2Z D.3X2+6Y2====2Z
Y2+2Z D.3X2+6Y2====2Z
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:阅读理解
| 容器 | A | B |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| CH3OH(g)浓度(mol?L-1) | c1 | c2 |
| 反应能量变化 | 放出29.4kJ | 吸收akJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 9.8 | 9.7 | 11.6 | 10.3 |
| 16 |
| 3 |
| 16 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.2X2+Y2====2Z B.X2+Y2====2Z
C.2X2![]() Y2+2Z D.3X2+6Y2====2Z
Y2+2Z D.3X2+6Y2====2Z
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西上饶中学高一零点、实验班下期末化学试卷(带解析) 题型:实验题
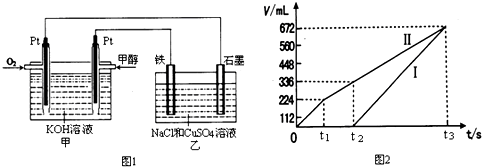
(12分)某研究小组为比较Al和Fe的金属性强弱,设计了图1所示的装置。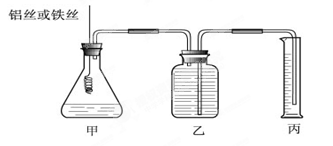
(1)甲中锥形瓶内盛放的液体是_______________________。
(2)若要比较产生气体的快慢,可以比较相同时间内产生气体的体积,也可以比较_ 。
(3)为了确保“Al和Fe的金属活动性不同是导致产生气体速率不同的唯一原因”,实验时需要控制好反应条件。实验时除需保证甲中液体的体积、物质的量浓度和温度相同外,还需保证___________。
(4)某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,盐桥中装有饱和K2SO4溶液.回答下列问题: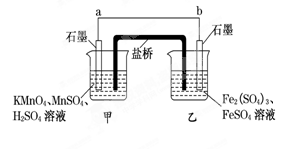
(注:盐桥常出现在原电池中,是由琼脂和和K2SO4溶液构成的,用来在两种溶液中转移电子。)
(i)发生氧化反应的烧杯是_______ (填“甲”或“乙”).
(ii)外电路的电流方向为:从______到____.(填“a”或“b”)
(iii)电池工作时,盐桥中的SO移向______(填“甲”或“乙”)烧杯.
(iv)甲烧杯中发生的电极反应式为_________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com