
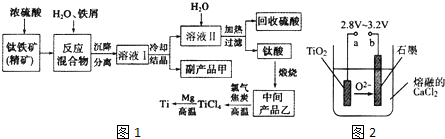
| �������� | Fe��OH��2 | TiO��OH��2 | Mg��OH��2 |
| Ksp | 8.0��10-14 | 1.0��10-29 | 1.8��10-11 |
���� ��������Ũ�����ܽ⣬��Ӧ����Ҫ������TiOSO4��FeSO4����������Һ�м������ˮϡ�ͺ����������ۻ�ԭ�����ӣ����˵õ���Һͨ������Ũ������ȴ�ᾧ�����˵õ���Һ�к��� Fe2+��TiO2+������Mg2+�������ӣ���ȴ�ᾧ�õ�����Ʒ��ҪΪFeSO4����Һ�м���ˮ���ȹ��˵õ�H2TiO3��H2TiO3�������յõ�TiO2����������������̼���¼��ȷ�Ӧ����TiCl4��һ����̼�����Ȼ��Ѻͽ���þ���¼��ȷ�Ӧ�õ��Ȼ�þ���ѽ�����
��1������ԭ���غ�ȷ�����������Ļ�ѧʽ������������ŨH2SO4��Ӧ�IJ���֮һ��TiOSO4��������FeSO4��ˮ��
��2������������ۻ�ԭ�����ӣ���ֹFe2+������ΪFe3+��
����������þ���ܶȻ�������Һ��OH-Ũ�ȣ��ٽ��ˮ�����ӻ�����c��H+��������pH=-lgc��H+�����㣻
TiO��OH��2���ܶȻ���С�������İ�ɫ����ΪTiO��OH��2��
��3����ΪTiO2��������������̼���¼��ȷ�Ӧ����TiCl4��һ����̼��Mg���������������������Ӧ����Ҫ����������
�����ѣ�Ti������Ӳ�ȴ��۵�ߡ�����ʱ����ʴ��������ϡ�������Mg��
��4������������ʯī����ʯīΪ������TiO2Ϊ�����������Ϸ�����ԭ��Ӧ����TiO2��õ�������Ti��O2-��
��� �⣺��������Ũ�����ܽ⣬��Ӧ����Ҫ������TiOSO4��FeSO4����������Һ�м������ˮϡ�ͺ����������ۻ�ԭ�����ӣ����˵õ���Һͨ������Ũ������ȴ�ᾧ�����˵õ���Һ�к��� Fe2+��TiO2+������Mg2+�������ӣ���ȴ�ᾧ�õ�����Ʒ��ҪΪFeSO4����Һ�м���ˮ���ȹ��˵õ�H2TiO3��H2TiO3�������յõ�TiO2����������������̼���¼��ȷ�Ӧ����TiCl4��һ����̼�����Ȼ��Ѻͽ���þ���¼��ȷ�Ӧ�õ��Ȼ�þ���ѽ�����
��1��������������R��ʾ����̼�ڸ����·�Ӧ�Ļ�ѧ����ʽΪ2R+C$\frac{\underline{\;����\;}}{\;}$2Fe+2TiO2+CO2��������ԭ���غ㣬���������Ļ�ѧʽΪ FeTiO3������������ŨH2SO4��Ӧ�IJ���֮һ��TiOSO4����Ӧ�����������ɣ�������FeSO4��ˮ���÷�Ӧ�Ļ�ѧ����ʽΪFeTiO3+2H2SO4$\frac{\underline{\;����\;}}{\;}$TiOSO4+FeSO4+2H2O��
�ʴ�Ϊ��FeTiO3��FeTiO3+2H2SO4$\frac{\underline{\;����\;}}{\;}$TiOSO4+FeSO4+2H2O��
��2������������ۻ�ԭ�����ӣ���ֹFe2+������ΪFe3+��
��Һ��Mg2+�����ʵ���Ũ��Ϊ0.0018mol/L������������þʱ����Һ��c��OH-��=$\sqrt{\frac{1.8��1{0}^{-11}}{0.0018}}$mol/L=10-4mol/L����c��H+��=10-10mol/L������ҺpH=-lgc��H+��=10��
TiO��OH��2���ܶȻ���С����Һ��ˮϡ�������İ�ɫ����ΪTiO��OH��2���÷�Ӧ�����ӷ���ʽΪ��TiO2++2H2O=TiO��OH��2����
�ʴ�Ϊ����ֹFe2+������ΪFe3+��10��TiO2++2H2O=TiO��OH��2����
��3����ΪTiO2��������������̼���¼��ȷ�Ӧ����TiCl4��һ����̼����Ӧ����ʽΪ��TiO2+2Cl2+2C$\frac{\underline{\;����\;}}{\;}$TiCl4+2CO��
Mg���������������������Ӧ����Ҫ�����������У�
�����ѣ�Ti������Ӳ�ȴ��۵�ߡ�����ʱ����ʴ��������ϡ�������Mg��
�ʴ�Ϊ��TiO2+2Cl2+2C$\frac{\underline{\;����\;}}{\;}$TiCl4+2CO������������ϡ���
��4������������ʯī����ʯīΪ������TiO2Ϊ��������bΪ��Դ�����������Ϸ�����ԭ��Ӧ����TiO2��õ�������Ti��O2-�������缫��ӦʽΪ��TiO2 +4e-=Ti+2O2-��
�ʴ�Ϊ������TiO2 +4e-=Ti+2O2-��
���� ���⿼���������������̣��漰İ������ʽ����д���Բ�����ԭ���ķ������ۡ����ԭ��Ӧ�õȣ����ؿ���ѧ�����Ķ���ȡ��Ϣ���������������������Ƕ�ѧ���ۺ������Ŀ��飬��Ŀ�ѶȽϴ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | �� | �� | ||||
| 3 | �� | �� | �� | �� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱZn �缫�������� | B�� | Zn �Ǹ�����Ag2O ������ | ||
| C�� | ����ʱ��Һ�е�����Ag2O ����Zn | D�� | ��Һ��������������Zn �缫�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
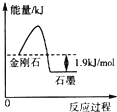 ���ݱ��е���Ϣ�ж�����˵��������ǣ�������
���ݱ��е���Ϣ�ж�����˵��������ǣ�������| ���� | ��� | ȼ����/��kJ•mol-1�� |
| ���ʯ | ��ɫ�������� | 395.4 |
| ʯī | �Һڣ��������� | 393.5 |
| A�� | �ɱ�����Ϣ�ɵ���ͼ��ʾ��ͼ�� | |
| B�� | �ɱ�����Ϣ֪C��ʯī��s��=C�����ʯ��s����H=+1.9 kJ•mol-1 | |
| C�� | �ɱ�����Ϣ��֪��ͬ�����½��ʯ���۵����ʯī���۵� | |
| D�� | ʯīȼ���ȵ��Ȼ�ѧ����ʽΪC��ʯī��s��+$\frac{1}{2}$O2��g���TCO��g����H=-393.5 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
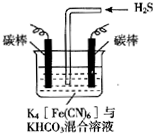 ���ԭ��������������Ⱦ�����й㷺��Ӧ�ã���ҵ�ϳ�������ͼ��ʾ���װ�ã��������Ļ�������[Fe��CN��6]3-�ɽ���̬�������е�����ת��Ϊ�����õ�������ת��Ϊ[Fe��CN��6]4-��ͨ���⣬Ȼ��ͨ��H2S���Դ���������˵������ȷ���ǣ�������
���ԭ��������������Ⱦ�����й㷺��Ӧ�ã���ҵ�ϳ�������ͼ��ʾ���װ�ã��������Ļ�������[Fe��CN��6]3-�ɽ���̬�������е�����ת��Ϊ�����õ�������ת��Ϊ[Fe��CN��6]4-��ͨ���⣬Ȼ��ͨ��H2S���Դ���������˵������ȷ���ǣ�������| A�� | ���ʱ������ӦʽΪ[Fe��CN��6]4--e-=[Fe��CN��6]3- | |
| B�� | ����������������Һ��pH��� | |
| C�� | ������������Ҫ���ϲ���K4[Fe��CN��6]��KHCO3 | |
| D�� | ͨ��H2Sʱ������Ӧ�����ӷ���ʽΪ��2[Fe��CN��6]3-+2CO32-+H2S=2[Fe��CN��6]4-+2HCO3-+S�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ�����������ǿ��ϡ���� | |
| B�� | ����ˮ��Ӧ�����ʣ�Na��Mg | |
| C�� | �����KI��Һ�е�����ˮ����Һ���� | |
| D�� | ԭ�Ӱ뾶��Al��Si��P |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
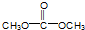 ���DMC�������ᡢ��ճ����ҵ�Ļ�������ɫ�ܼ���DMC�ĺϳɷ����ܶ࣬������ϩΪԭ�ϣ���״������������ĺϳ�·�����£�
���DMC�������ᡢ��ճ����ҵ�Ļ�������ɫ�ܼ���DMC�ĺϳɷ����ܶ࣬������ϩΪԭ�ϣ���״������������ĺϳ�·�����£�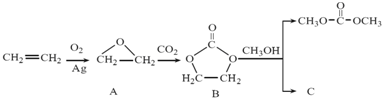

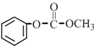 ��
��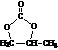 �ĺϳ�·�ߣ�ע����Ҫ�ķ�Ӧ������
�ĺϳ�·�ߣ�ע����Ҫ�ķ�Ӧ������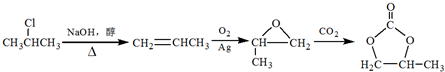 ���ϳ�·�߳��õı�ʾ��ʽΪ��A$��_{��Ӧ����}^{��Ӧ�Լ�}$B��$��_{��Ӧ����}^{��Ӧ�Լ�}$Ŀ����
���ϳ�·�߳��õı�ʾ��ʽΪ��A$��_{��Ӧ����}^{��Ӧ�Լ�}$B��$��_{��Ӧ����}^{��Ӧ�Լ�}$Ŀ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
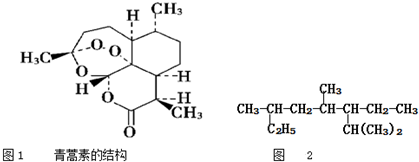
| A�� | �������ʵķе㰴�ɵ͵��ߵ�˳������ΪCH3��CH2��2CH3��CH3��CH2��3CH3����CH3��3CCH3����CH3��2CHCH2CH3 | |
| B�� | �������ǿ�ű����Чҩ���ṹ��ͼ1��ʾ�������������������Ѽ���������ˮ���������ȷ¡���ͪ�ȣ����������Ѵ�ֲ������ȡ���ܹ�����ˮ�ⷴӦ������ǿ������ | |
| C�� | ��֬��һ��������ˮ��ɸ�֬������ͣ���Ϊ������Ӧ | |
| D�� | ��ϵͳ����������ʱ��ͼ2�л����������3��5��7-����-6-�һ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com