
| 待测液 | 消耗标准盐酸(0.1000mol/L)的体积 | |
| ① | 20.00mL NaOH溶液 | V1 mL |
| ② | 20.00mL NaOH溶液+10.00mL水 | V2 mL |
| ③ | 敞口隔夜放置的20.00mL NaOH溶液 | V3 mL |
| A. | c=0.1000×$\frac{{V}_{1}+{V}_{2}+{V}_{3}}{3×20.00}$ | B. | c=0.1000×$\frac{{V}_{1}+{V}_{2}}{2×20.00}$ | ||
| C. | c=0.1000×$\frac{{V}_{1}+{V}_{3}}{2×20.00}$ | D. | c=$\frac{0.1000{V}_{1}}{20.00}$ |
分析 ③中NaOH溶液敞口放置,NaOH与空气中CO2反应造成NaOH减少,生成Na2CO3,而用盐酸滴定Na2CO3溶液,反应分两个阶段进行:①H++CO32-=HCO3-(此时溶液呈弱碱性),②H++HCO3-=CO2↑+H2O,酚酞的变色范围为pH在8到10之间,滴定反应按①进行,会导致消耗盐酸的量减少,故不能用V3 mL计算,为减少误差,应多次重复实验,取平均值,故选择①②数据计算消耗盐酸的平均体积,再根据c(NaOH)×V(NaOH溶液)=c(HCl)×V(盐酸)计算.
解答 解:敞口隔夜放置,NaOH与CO2反应生成Na2CO3,而用盐酸滴定Na2CO3溶液,反应分两个阶段进行:①H++CO32-=HCO3-(此时溶液呈弱碱性),②H++HCO3-=CO2↑+H2O,酚酞的变色范围为pH在8到10之间,滴定反应按①进行,导致消耗盐酸的量减少,所以第三组实验数据不能使用,故V3应该舍弃,A、C项错误;
为减少误差,多次重复实验,应取平均值,D项错误;
选择①②数据计算,消耗盐酸的平均体积为:$\frac{{V}_{1}+{V}_{2}}{2}$mL,
根据c(NaOH)×V(NaOH溶液)=c(HCl)×V(盐酸),可得c(NaOH)×20mL=0.1000mol/L×$\frac{{V}_{1}+{V}_{2}}{2}$mL,
解得:c(NaOH)=0.1000×$\frac{{V}_{1}+{V}_{2}}{2×20}$mol/L,
故选B.
点评 本题考查物质的量浓度计算、酸碱中和滴定等,题目难度中等,注意掌握中和滴定操作方法,明确根据滴定数据计算物质的量浓度的方法,试题培养了学生灵活应用知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+═2Fe3++2H2O | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O | |
| C. | 少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O═2C6H5OH+CO32- | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
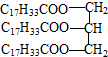 .从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是
.从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是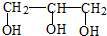 (写结构简式).
(写结构简式).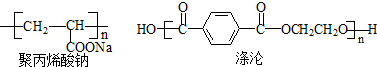
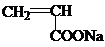 ,反应类型是加聚反应;
,反应类型是加聚反应;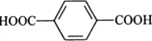 ,其核磁共振氢谱的峰面积比是1:2(或2:1).
,其核磁共振氢谱的峰面积比是1:2(或2:1).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 六水氯化钙属于混合物 | B. | 葡萄糖注射液不能产生丁达尔效应 | ||
| C. | 食盐水属于浊液 | D. | 氯化铵不属于盐类 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.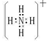 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(3) | B. | (2)(4) | C. | (1)(4)(5) | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是含有碳元素的化合物都属于有机物 | |
| B. | 大多数有机物都是由分子构成的 | |
| C. | 有机物都很容易燃烧 | |
| D. | 易溶于汽油、酒精、苯等有机溶剂中的物质,一定是有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③⑤ | C. | ①④⑤ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com