
 H2O2+
H2O2+ 6H+=
6H+= Mn2++
Mn2++ O2↑+
O2↑+ 8H2O;
8H2O;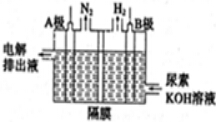
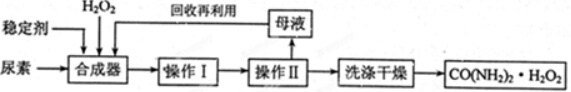
分析 (1)因为过氧化尿素具有尿素和过氧化氢双重性质,受热易分解,所以应使溶液在较低温度下蒸发,因此操作I、II的名称分别是低温蒸发、过滤;CO(NH2)2•H2O2分子中尿素和过氧化氢都已经达到稳定结构,二者之间的结合力较弱,应该为氢键;
(2)首先写出CH4与H2O反应的化学方程式并注明状态,然后根据盖斯定律求焓变,可得热化学方程式.
(3)①根据氧化还原反应中,化合价升高的价数和降低相等,MnO4?中Mn元素降低5价,H2O2中O元素升高1价,所以MnO4?和Mn2+的系数为2,H2O2和O2的系数为5,然后利用观察法配平化学方程式.
②根据反应时KMnO4与H2O2的物质的量之比为2:5,可得产品中H2O2的质量分数=0.2mol/L×0.02L×5/2×10×34g/mol÷12g×100%=28.3%
(4)根据图示,B极发生H+得电子生成H2,所以B为阴极,连接电源的负极;阳极CO(NH2)2失去电子转化为N2,因为电解液含KOH,所以电极方程式为:CO(NH2)2-6e-+8OH-═N2↑+CO32-+6H2O.
解答 解:(1)因为过氧化尿素具有尿素和过氧化氢双重性质,受热易分解,所以应使溶液在低温蒸发浓缩,冷却结晶,因此操作I、II的名称分别是低温蒸发浓缩,冷却结晶,过滤;CO(NH2)2•H2O2分子中尿素和过氧化氢都已经达到稳定结构,二者之间的结合力较弱,应该为氢键;
故答案为:低温蒸发浓缩,冷却结晶;过滤;氢键;
(2)首先写出CH4与H2O反应的化学方程式并注明状态,然后根据盖斯定律求焓变,△H=-890.3kJ•mol?1+4×285.8kJ•mol?1-2×44kJ•mol?1 =+164.9 kJ•mol?1,可得热化学方程式为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+164.9 kJ/mol;
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+164.9 kJ/mol;
(3)①根据氧化还原反应中,化合价升高的价数和降低相等,MnO4?中Mn元素降低5价,H2O2中O元素升高1价,所以MnO4?和Mn2+的系数为2,H2O2和O2的系数为5,然后利用观察法配平化学方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O;
故答案为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O;
②根据2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,反应时KMnO4与H2O2的物质的量之比为2:5,可得产品中H2O2的质量分数=0.2mol/L×0.02L×$\frac{5}{2}$×10×34g/mol÷12g×100%=28.3%;
故答案为:28.3%;
(4)根据图示,阳极CO(NH2)2失去电子转化为N2,因为电解液含KOH,所以电极方程式为:CO(NH2)2-6e-+8OH-═N2↑+CO32-+6H2O;
故答案为:CO(NH2)2-6e-+8OH-=N2↑+CO32-+6H2O.
点评 本题考查了物质分离方法,化学方程式计算,有机物质结构分析判断,离子方程式书写,实验 过程分析和电解池原理的理解应用是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 选项 | 叙述I | 叙述II |
| A. | KNO3的溶解度大 | 用重结晶法除去KNO3中混有的NaCl |
| B. | BaSO4难溶于酸 | 用盐酸和BaCl2溶液检验SO42- |
| C. | NH3能使酚酞溶液变红 | NH3可用于设计喷泉实验 |
| D. | Ca(OH)2能制成澄清石灰水 | 可配制2.0 mol?L-1的Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ③④⑤ | C. | ②④⑤ | D. | ②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | Ⅵ | VⅡA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
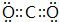 ,写出它的一种用途做灭火剂等.
,写出它的一种用途做灭火剂等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
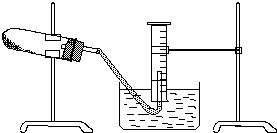 某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下:
某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3)3CCH2CH3 | ||
| C. | (CH3)2CHCH2CH2CH(CH3)2 | D. | (CH3)2CHCH2CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com