
| A. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| B. | 某温度下,2L密闭容器中加入4mol A和2mol B发生反应: 3A(g)+2B(g)?4C(s)+2D(g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=$\frac{{c}^{4}(C){c}^{2}(D)}{{c}^{3}(A){c}^{2}(B)}$ | |
| C. | 温度一定时,当溶液中c(Ag+)•c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | |
| D. | 难溶电解质AB2饱和溶液中,c(A2+)=x mol•L-1,c(B-)=y mol•L-1,则Ksp值为4xy2 |
分析 A.平衡常数是用生成物浓度的幂次方乘积除以反应物的幂次方乘积计算,和化学方程式书写有关;
B.固体和液体不写入平衡常数表达式中;
C.沉淀溶解平衡状态下离子浓度幂次方乘积等于Ksp达到沉淀溶解平衡,形成饱和溶液;
D.依据沉淀溶解平衡状态下饱和溶液中离子浓度的幂次方乘积计算Ksp.
解答 解:A.平衡常数是用生成物浓度的幂次方乘积除以反应物的幂次方乘积计算,和化学方程式书写有关,系数变化,平衡常数变化,故A错误;
B.固体和液体不写入平衡常数表达式中,3A(g)+2B(g)?4C(s)+2D( g).平衡常数K=$\frac{{c}^{2}(D)}{{c}^{3}(A){c}^{2}(B)}$,故B错误;
C.沉淀溶解平衡状态下离子浓度幂次方乘积等于Ksp达到沉淀溶解平衡,形成饱和溶液,温度一定时,当溶液中(Ag+)•c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液,故C正确;
D.沉淀溶解平衡状态下饱和溶液中离子浓度的幂次方乘积计算Ksp,AB2饱和溶液中AB2(s)?A2+(aq)+2B-(aq),Ksp=c(A2+)c2(B-)=xy2,故D错误.
故选C.
点评 本题考查了平衡常数的分析判断主要是表达式书写,为高频考点,侧重于学生的分析能力的考查,题目涉及沉淀溶解平衡的理解应用,溶度积常数计算式,题目难度中等.


科目:高中化学 来源:2016-2017学年安徽师大附中高二上10月月考化学卷(解析版) 题型:选择题
一定条件下溶液的酸碱性对TiO2光催化燃料R降解反应的影响如图所示。下列判断正确的是
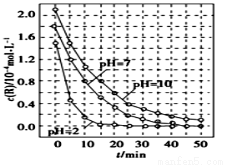
A.溶液酸性越强,R 的降解速 率越小
率越小
B.R的起始浓度越小,降解速率越大[
C.在0~50 min之间,pH=2和PH=7时R的降解百分率相等
D.在20~25 min之间,pH=10 时R的平均降解速率为0.04 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
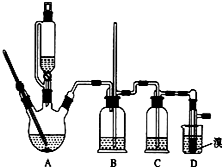 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
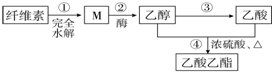
| A. | ③和④都发生了氧化还原反应 | |
| B. | M虽然分子结构中无醛基,但仍然可以发生银镜反应 | |
| C. | 步骤②,1molM完全反应可以生成3mol乙醇 | |
| D. | 若用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
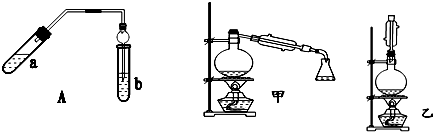
| 实验编号 | 试管a中试剂 | 试管b中试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL18mol•L-1 浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
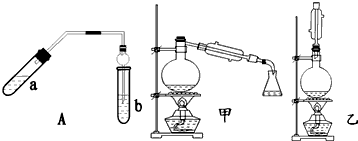
| 实验编号 | 试管a中试剂 | 试管b中试剂 | 测得有机层 的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL18mol•L-1浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com