
【题目】(1)已知拆开1mo1H-H键、1molN≡N键、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。则生成1mo1 NH3时反应放出______________kJ 的热量。
(2)天然气既是高效洁净的能源,也是重要的化工原料。
①甲烷分子的结构式为_________,空间构型为_______________。
②甲烷高温分解生成氢气和炭黑。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是__________________________________________。
(3)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的的是________(填序号)。

(4)直接乙醇燃料电池(DEFC)具有很多优点,引起了人们的研究兴趣。现有以下三种乙醇燃料电池。

①三种乙醇燃料电池中正极反应物均为______________________;
②碱性乙醇燃料电池中,电极a上发生的电极反应式为_______________________;
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,电极b上发生的电极反应式为_______________________________________________。
【答案】46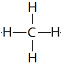 正四面体提供甲烷分解所需的能量②O2C2H5OH+16OH--12e-=2CO32-+11H2OO2+2CO2+4e-=2CO32-
正四面体提供甲烷分解所需的能量②O2C2H5OH+16OH--12e-=2CO32-+11H2OO2+2CO2+4e-=2CO32-
【解析】
(1)已知拆开1mo1H-H键、1molN≡N键、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ,根据反应热等于断键吸收的能量和形成化学键放出的能量的差值,则生成2mol氨气放出的热量是2×3×391kJ-3×436kJ-946kJ=92kJ,所以生成1mo1 NH3时反应放出46kJ的热量。
(2)①甲烷分子的化学式为CH4,结构式为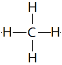 ,空间构型为正四面体。
,空间构型为正四面体。
②由于甲烷高温分解需要吸收能量,所以进行此反应时要通入适量空气使部分甲烷燃烧的目的是提供甲烷分解所需的能量。
(3)验证Fe3+与Cu2+氧化性强弱,在原电池中,铜作负极、其它导电的金属或非金属作正极,电解质溶液为可溶性的铁盐,则
①中铁作负极、Cu作正极,电池反应式为Fe+2Fe3+=3Fe2+,不能验证Fe3+与Cu2+氧化性强弱,错误;
②中铜作负极、银作正极,电池反应式为Cu+2Fe3+=Cu2++2Fe2+,能验证Fe3+与Cu2+氧化性强弱,正确;
③中铁发生钝化现象,Cu作负极、铁作正极,电池反应式为:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,不能验证氧化性强弱,错误;
④中铁作负极、铜作正极,电池反应式为:Fe+Cu2+=Cu+Fe2+,不能验证Fe3+与Cu2+氧化性强弱,错误;
答案选②。
(4)①燃料电池中正极均是氧气得到发生还原反应,因此三种乙醇燃料电池中正极反应物均为O2;
②碱性乙醇燃料电池中,电极a上通入的是乙醇,乙醇发生失去电子的氧化反应转化为碳酸盐,则发生的电极反应式为C2H5OH+16OH--12e-=2CO32-+11H2O;
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,电极b上通入的是空气,氧气得到电子,由于负极产生的二氧化碳部分进入正极,则正极发生的电极反应式为O2+2CO2+4e-=2CO32-。


科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍 (Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示。下列说法正确的是
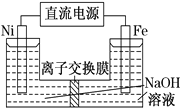
A. 铁是阳极,电极反应为Fe-2e-+2OH-===Fe(OH)2↓
B. 电解一段时间后,镍电极附近溶液的pH减小
C. 每制得1 mol Na2FeO4,理论上可以产生67.2L气体
D. 若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol/L的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。
(1)原NaOH溶液的质量分数为
(2)所得溶液中Cl-的物质的量为 mol
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2):n(H2)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质:①氯化氢气体 ②氨气 ③金属钠 ④ 硝酸钾⑤ 酒精⑥ 氢氧化钠溶液(用编号回答)其中属于电解质的有__;其中属于非电解质的有__;能导电的物质__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的说法中正确的是( )
A.氧化还原反应过程中一定有电子转移
B.氧化还原反应前后一定有氧的得失
C.实现Fe3+→Fe2+的变化过程失去电子
D.失去电子的反应是还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某兴趣小组根据教材实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验。请观察如下图所示实验装置,分析实验原理,并判断下列说法和做法,其中不科学的是( )

A. 甲为小苏打,乙为纯碱
B. 要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C. 加热不久就能看到A烧杯的澄清石灰水变浑浊
D. 整个实验过程中都没有发现A烧杯的澄清石灰水变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温下的密闭容器中,有可逆反应2NO(g)+O2(g)![]() 2NO2(g);ΔΗ<0,不能说明已达到平衡状态的是
2NO2(g);ΔΗ<0,不能说明已达到平衡状态的是
A. 正反应生成NO2的速率和逆反应生成O2的速率相等
B. 混合气体颜色深浅保持不变
C. 反应器中压强不随时间变化而变化
D. 混合气体平均分子量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 元素周期表中,除第一和第七周期外,第n周期所含非金属元素(包括稀有气体元素)的种数均为(8-n)
B. SiCl4、PCl3分子中各原子最外层均达到8电子稳定结构
C. M层电子数为奇数的主族元素所在族的序数与该元素原子的M层电子数不一定相等
D. 由ⅠA族和ⅥA族短周期元素形成的原子个数比为1∶1,电子总数为38的化合物,是含有共价键的离子型化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com