
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
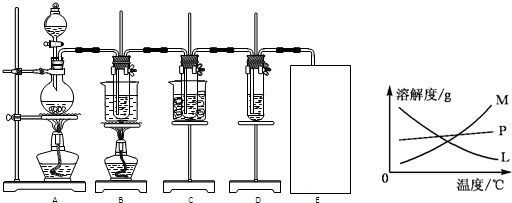
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
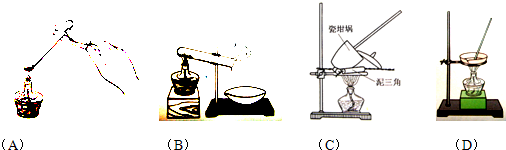
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g/100g水 | 18.5 | 20.8 | 26.3 | 32.8 | 40.1 | 48.4 | 52.4 | 50.9 | 43.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:
(6分)实验室进行下列实验:①制乙烯 ②制乙炔 ③石油分馏 ④苯的硝化 ⑤制溴苯 ⑥制乙酸乙酯
(1)不需要加热的有__________________;
(2)需要水浴的有____________________;
(3)需要用温度计的有_______;其中温度计插入反应液中的有______;
(4)需加催化剂的有__________________;
(5)加入浓H2SO4且起催化剂、脱水剂作用的有________________。
查看答案和解析>>
科目:高中化学 来源:2010年黑龙江省五大连池市高级中学等五校联谊高二下学期期末考试 题型:实验题
(6分)实验室进行下列实验:①制乙烯 ②制乙炔 ③石油分馏 ④苯的硝化 ⑤制溴苯 ⑥制乙酸乙酯
(1)不需要加热的有__________________;
(2)需要水浴的有____________________;
(3)需要用温度计的有_______;其中温度计插入反应液中的有______;
(4)需加催化剂的有__________________;
(5)加入浓H2SO4且起催化剂、脱水剂作用的有________________。
查看答案和解析>>
科目:高中化学 来源:2010年黑龙江省五大连池市等五校联谊高二下学期期末考试 题型:实验题
(6分)实验室进行下列实验:①制乙烯 ②制乙炔 ③石油分馏 ④苯的硝化 ⑤制溴苯 ⑥制乙酸乙酯
(1)不需要加热的有__________________;
(2)需要水浴的有____________________;
(3)需要用温度计的有_______;其中温度计插入反应液中的有______;
(4)需加催化剂的有__________________;
(5)加入浓H2SO4且起催化剂、脱水剂作用的有________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com