
【题目】一定条件下的2L密闭容器,进行反应2X(g)+Y(g) ![]() 2Z(g),若起始时X、Y、Z物质的量分别为n1、n2、n3(均不为零)。达平衡时,X、Y、Z浓度分别为0.2mol/L、0.1 mol /L和0.08 mol/L,则下列判断合理的是( )
2Z(g),若起始时X、Y、Z物质的量分别为n1、n2、n3(均不为零)。达平衡时,X、Y、Z浓度分别为0.2mol/L、0.1 mol /L和0.08 mol/L,则下列判断合理的是( )
A. X和Y的转化率不一定相等
B. n1、n2=2:1
C. 平衡时,Y和Z的生成速率之比为2:1
D. n1的取值范围为0<n1<0.28
科目:高中化学 来源: 题型:
【题目】高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿制高锰酸钾的流程如下:

请回答下列问题:
(1)KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是 (填代号).
a.84消毒液(NaClO溶液) b.双氧水 c.苯酚 d.75%酒精
(2)操作Ⅰ的名称是___________________;操作Ⅱ根据KMnO4和K2CO3两物质在溶解性上的差异,采用________________(填操作步骤)、趁热过滤得到KMnO4粗晶体.
(3)写出二氧化锰和氢氧化钾熔融物中通入空气时发生的主要化学反应的方程式: 。
(4)以惰性材料为电极,采用电解锰酸钾溶液的方法也可制得高锰酸钾,则阳极反应式为 。
(5)测定高锰酸钾样品纯度:向高锰酸钾溶液中滴定硫酸锰溶液,产生黑色沉淀。当溶液由紫红色刚好褪色且半分钟不变色,表明达到滴定终点。写出离子方程式: 。
(6)理论上(若不考虑物质循环与制备过程中的损失)1mol MnO2可制得 mol KMnO4.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,向500℃左右的铁屑中通入Cl2生产无水氯化铁,其制备过程中均要确保无水。现模拟该过程用图示装置进行实验:

(1)仪器a的名称为________,装置A的圆底烧瓶中发生反应的化学方程式为________,为保持装置C为无水环境,装置B中加入的试剂是________。
(2)实验步骤:如图连接装置后,先________(填实验操作),再装药品,然后点燃________(填“A”或“C”)处酒精灯,当________(填实验现象)时,再点燃________(填“A”或“C”)处酒精灯。
(3)装置D的作用是________,________。
(4)甲同学认为进入装置C的气体中混有HCl,应在装置B前增加装有________(填试剂名称)的洗气装置除去;乙同学认为不需要除去HCl,理由为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备单质硅时,主要化学反应如下:①SiO2+2C=Si+2CO↑;②Si+2Cl2=SiCl4;③SiCl4+2H2=Si+4HCl。下列对上述三个反应的叙述中,不正确的是( )
A.①③为置换反应
B.①②③均为氧化还原反应
C.②为化合反应
D.三个反应的反应物中硅元素均被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.理论上任何氧化还原反应都可以设计成原电池。
B.甲烷的标准燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g)△H=-38.6 kJ/mol
2NH3(g)△H=-38.6 kJ/mol
D.同温同压下,等量的氢气完全发生反应:H2(g)+Cl2(g)=2HCl(g),在点燃条件下放出的热量与光照条件下放出的热量相等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式,书写正确的是( )
A. Al2(SO4)3=2Al3++ 3SO42- B. AlCl3= Al3++Cl-
C. Mg(NO3)2= Mg+2+2NO3- D. KMnO4=K++Mn7++4O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生产和生活中,金属材料几乎无处不在。
(1)铝是一种活泼金属,具有较强的还原性。
①金属铝在高温下与三氧化二铁反应,2Al+Fe2O3=Al2O3+2Fe,称为铝热反应。试 用双线桥法表示电子转移情况:____________________。
②能否用铝制容器盛装NaOH溶液?________(填“能”或“不能”),
(2)将镁、铝的混合物共0.2 mol,溶于200 mL 4 mol·L﹣1的盐酸溶液中,然后再滴加2 mol·L﹣1的NaOH溶液。请回答下列问题:
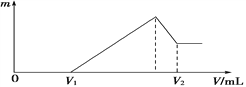
①若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示。当V1=160 mL时,则金属粉末中n (Al)=________________________mol。
②0~V1段发生的反应的离子方程式为______________________________;
③若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=_____________mL;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.能电离出氢离子的化合物叫做酸
B.能电离出氢氧根离子的化合物叫做碱
C.能电离出酸根离子的化合物叫做盐
D.由金属离子和酸根离子组成的化合物属于盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com