
| A. | C14H18O5 | B. | C14H22O3 | C. | C16H26O5 | D. | C16H20O3 |
科目:高中化学 来源: 题型:填空题
| 序号 | 温度 | 0.1mol•L-1Na2S2O3溶液 | 0.1mol•L-1H2SO4溶液 | H2O | 达到相同程度所用的时间/s |
| ① | 25℃ | 25mL | 25mL | 0mL | 4 |
| ② | 25℃ | 25mL | 15mL | 10.0mL | 6 |
| ③ | 25℃ | V1 | 25mL | 10mL | 6 |
| ④ | 45℃ | V2 | 25mL | V3 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为防止被氧化,FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| B. | 将金属Li放于石蜡中密封保存 | |
| C. | 将NaOH溶液存放于磨口玻璃塞的试剂瓶 | |
| D. | 硝酸应装在棕色瓶中密封避光保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多 | |
| B. | 第二周期元素从Li到F,金属性逐渐减弱,非金属性逐渐增强 | |
| C. | 因为Na比K容易失去电子,所以Na比K的还原性强 | |
| D. | O与S为同主族元素,且O比S的非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤②①④③ | B. | ⑤①②③④ | C. | ④③②①⑤ | D. | ④③①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X3YZ4 | B. | X2YZ3 | C. | XYZ4 | D. | X2YZ4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
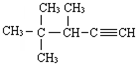 的系统名称为( )
的系统名称为( )| A. | 2,2,3一三甲基一1-戊炔 | B. | 3,4,4一三甲基一l一戊炔 | ||
| C. | 3,4,4一三甲基-2一戊炔 | D. | 2,2,3一三甲基一4一戊炔 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com