
| A、②③⑤ | B、①④⑥ |
| C、③④⑤ | D、②④⑥ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
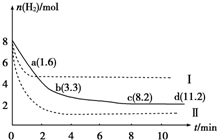 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是( )
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是( )| A、该反应在低温条件下能自发进行 |
| B、曲线Ⅰ改变的条件可能是升高温度 |
| C、若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是:K2>K>K1 |
| D、容器内气体平均摩尔质量不再改变说明该反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用10 mL 量筒量取5.2 mL盐酸 |
| B、用广泛pH试纸测得某溶液的pH值为12.5 |
| C、用托盘天平称取25.12gNaCl固体 |
| D、用100 mL容量瓶配制50mL0.1 mol/L的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.250 mol |
| B、0.125 mol |
| C、0.100 mol |
| D、0.080 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某放热反应在一定温度下不能自发进行,则该反应的体系混乱度减小 |
| B、NH4F溶液能存放于玻璃试剂瓶中 |
| C、海底蕴藏着大量的可燃冰,在通常情况下能稳定存在 |
| D、酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲~丁是含同一种元素的四种物质,甲和丁分别是该元素的单质和最高价氧化物的水化物,它们之间有如图所示的转化关系,甲不可能是( )
甲~丁是含同一种元素的四种物质,甲和丁分别是该元素的单质和最高价氧化物的水化物,它们之间有如图所示的转化关系,甲不可能是( )| A、Fe | B、Si | C、Al | D、S |
查看答案和解析>>
科目:高中化学 来源: 题型:
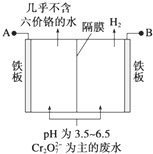 某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴阳极,槽中盛放含铬废水,原理示意图如图,下列说法正确的是( )
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴阳极,槽中盛放含铬废水,原理示意图如图,下列说法正确的是( )| A、A电源的负极 |
| B、阳极区溶液中发生的氧化还原反应为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O |
| C、阴极区附近溶液的pH降低 |
| D、若不考虑气体的溶解,当收集到H213.44L时有0.1molCr2O72-被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com