
下图是一些重要工业生产的转化关系(反应条件略去)。
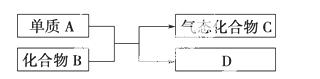
请完成下列问题:
(1)若D是单质,且与A属于同一主族,则:
①反应的化学方程式是_____________________________________________
_______________________________。
②D的原子结构示意图是________。
③D单质的一种重要用途是__________________________________________
_________________________________________。
(2)若B为黄色固体,D为固体化合物,则:
①该反应的化学方程式是____________________________________________
____________________________________。
②生产该工业品的工厂应建在离________较近的地方。
③实验室检验C的方法是____________________________________________
_________________ ______________________。
______________________。
(3)若B是一种有刺激性气味的气体,则 :
:
①B分子的空间构型为________。
②实验室进行此实验时,常看到有大量白烟 产生,产生大量白烟的原因是____________________________________________________________。
产生,产生大量白烟的原因是____________________________________________________________。
③化合物C在一定体积的容器中,在一定条件下发生反应,测得容器内气体的压强略小于原来的。请写出该反应的化学方程式_______________________________________。
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴已知4NH3(g)+5O2(g)=4NO(g) +6H2O(l),△H=x kJ/mol。蒸发1mol 液态水需要吸收的能量为44kJ,其它相关数据如下表:
| NH3(g) | O2(g) | NO(g) | H2O(g) | |
| 1mol分子断裂化学键时需要吸收的能量/kJ | a | b | z | d |
则表中z(用x、a、b、d表示)的大小为______________________________________________
⑵已知a g 乙烯气体充分燃烧时生成1molCO2和液态水,放出b k J的热量,则乙烯燃烧热的热化学方程式为________________________________________________。
⑶利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可以制备CuSO4,若将该反应设计为原电池,其正极电极反应式为 。
⑷肼(N2H4)—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。该电池放电时,负极的电极反应式是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中有6瓶失去标签的白色固体:纯碱、氢氧化镁、氯化钡、硫酸铝、硫酸氢钠、氯化钾。除蒸馏水、试管和胶头滴管外,无其他任何试剂和仪器。某学生通过以下实验步骤即可鉴别它们。请填写下列空白:
(1)各取适量固体于6支试管中,分别加入适量蒸馏水,有一支试管中的现象和其他5支明显不同,此试管中的现象是______________________________________________,
据此现象鉴别出的一种物质是__________。
(2)分别将所剩5种溶液依次编号为A、B、C、D、E,然后进行两两混合。观 察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
①A、C、D三种物质的化学式依次是_______________________________________。
②B、E两者中有一种可与A反应,它与足量A反应的离子方程式为________ ____。
____。
③在两两混合时,能最终确定B、E成分的实验现象及结论是_____________________。
(3)上述物质溶于水抑制水的电离,且溶液显酸性的物质的化学式为________,其溶液显酸性的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A~M为中学化学的常见物质,它们之间的转化关系如图所示,部分生成物和反应条件省略。已知C、D是由元素X、Y、Z中的两种组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子 最外层电子数之和为10。D为无色气体且不能燃烧,G为黄绿色单质气体,J、M为金属,
最外层电子数之和为10。D为无色气体且不能燃烧,G为黄绿色单质气体,J、M为金属, I有漂白作用,反应①常用于制作印刷电路板。请回答
I有漂白作用,反应①常用于制作印刷电路板。请回答 下列问题:
下列问题:
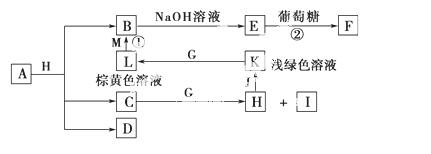
(1)写出A的化学式:____________。
(2)比较Y与Z的原子半径大小:_______ _>________(填元素符号)。
_>________(填元素符号)。
(3)检验L溶液中金属阳离子的方法是_ ___________________________
___________________________
____________________________________________。
(4)已知F溶于稀硝酸,溶液变成蓝色,放出无色气体。请写出该反应的化学方程式:_________________________________________________________
_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下除去杂质所选择的试剂和关键操作都正确的是( )
A. 硝基苯中含有少量的硫酸和硝酸:加入水;洗涤,过滤
B. 溴苯中含有少量溴:加入苯;萃取、分液
C. 乙酸乙酯中含有少量乙酸:加入酒精和浓硫酸;加热反应除去
D. 酒精中含有少量水:加入生石灰;蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+H+,下列说法正确的是( )
A.H2O2的氧化氢比Fe3+强,其还原性比Fe2+弱
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中, Fe2+和Fe3+的总量保持不变
D.H2O2生产过程要严格避免混入Fe2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com