
分析 根据三行式,结合平衡常数和反应速率的公式来求解,
A的初始浓度0.050mol•L-1,5min后反应达到平衡,A的转化率为70%,消耗A的浓度=0.050mol•L-1×70%=0.035mol,
A(g)?B(g)+C(g)
起始浓度:0.050 0 0
变化浓度:0.035 0.035 0.035
平衡浓度:0.015 0.035 0.035
(1)利用平衡浓度总和和体积计算平衡混合气体总物质的量;
(2)反应速率v=$\frac{△c}{△t}$计算得到.
解答 解:A的初始浓度0.050mol•L-1,5min后反应达到平衡,A的转化率为70%,消耗A的浓度=0.050mol•L-1×70%=0.035mol,
A(g)?B(g)+C(g)
起始浓度:0.050 0 0
变化浓度:0.035 0.035 0.035
平衡浓度:0.015 0.035 0.035
(1)平衡时体系总的物质的量为=(0.015+0.035+0.035)mol/L×1L=0.085mol,
故答案为:0.085mol;
(2)反应在0~5min区间的平均反应速率v(A)=$\frac{0.035mol/L}{5min}$=0.007mol/(L•min);
故答案为:0.007mol/(L•min).
点评 本题考查了化学反应速率计算,主要是三行计算的应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:填空题
 ;
;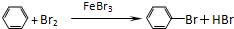 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
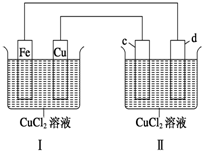
| A. | Ⅰ和Ⅱ无外加电源,都是原电池 | |
| B. | 铁为负极,d为阴极,两个电极上都发生还原反应 | |
| C. | Ⅰ中铜电极Ⅱ中c电极上有铜析出 | |
| D. | Ⅰ是原电池,Ⅱ是电解池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、苯、乙醇均能使酸性高锰酸钾溶液褪色 | |
| B. | 乙烯和聚丙烯都能与氢气在一定条件下发生加成反应 | |
| C. | 煤制煤气是化学变化,是高效、清洁地利用煤的重要途径 | |
| D. | 乙酸乙酯、油脂、葡萄糖、蛋白质都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
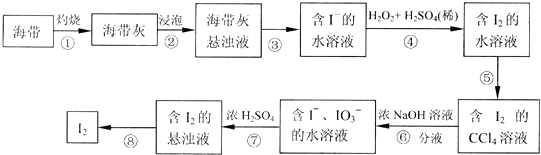
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
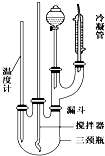 硝基苯是一种重要的化工原料,其制备原理是:
硝基苯是一种重要的化工原料,其制备原理是: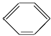 +HO-NO2$→_{50~60℃}^{H_{2}SO_{4}}$
+HO-NO2$→_{50~60℃}^{H_{2}SO_{4}}$ 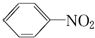 +H2O△H<0
+H2O△H<0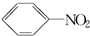 +HO-NO2$→_{△}^{H_{2}SO_{4}}$
+HO-NO2$→_{△}^{H_{2}SO_{4}}$ 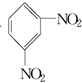 +H2O
+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强(对于气体反应),活化分子总数必然增大,故反应速率增大 | |
| B. | 温度升高,分子动能增加,减小了活化能,故反应速率增大 | |
| C. | 选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 | |
| D. | H+和OH-的反应活化能非常小,反应几乎在瞬间完成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com