
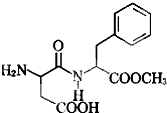
 阿斯巴甜具有清爽的甜味,其结构简式如图所示.下列关于阿斯巴甜的说法中,不正确的是( )
阿斯巴甜具有清爽的甜味,其结构简式如图所示.下列关于阿斯巴甜的说法中,不正确的是( )| A、一定条件下可以发生酯化反应和加成反应 |
| B、完全水解,生成两种有机物 |
| C、阿斯巴甜属于糖类化合物 |
| D、在酸性条件下可以水解生成两种氨基酸 |


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
| A、纯水在25℃和100℃时的pH |
| B、CH3COONa溶液中Na+和CH3COO-的浓度 |
| C、相同温度下,0.1 mol/LCH3COOH溶液和0.3 mol/LCH3COOH溶液的电离平衡常数 |
| D、用0.1 mol/LNaOH溶液分别中和pH、体积均相同的盐酸和醋酸,所消耗NaOH溶液的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓H2SO4 |
| 170℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可用铁氰酸钾溶液检验硫酸亚铁铵溶液中的亚铁离子 |
| B、可用淀粉溶液检验海带灰浸出液中的碘元素 |
| C、可用纸层析法分离铁离子与铜离子,分离时,蓝色斑点在棕色斑点的下方,说明铜离子在固定相中分配得更多 |
| D、过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离方法 |
查看答案和解析>>
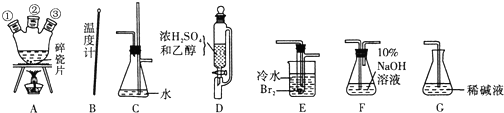
科目:高中化学 来源: 题型:
| A、②④⑤ | B、①④⑤ |
| C、③④ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、等物质的量浓度的各溶液pH关系为pH(CH3COONa)>pH(Na2CO3)>pH(NaCN) |
| B、a mol?L-1HCN溶液与b mol?L-1 NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定小于b |
| C、0.1 mol?L-1CH3COOH溶液中逐滴加入水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
| D、NaHCO3和Na2CO3混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
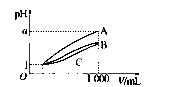 pH=1的三种酸溶液A、B、C各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )
pH=1的三种酸溶液A、B、C各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )| A、溶液的物质的量浓度C>B>A |
| B、酸性A>B>C |
| C、若a=4,则A是强酸,B、C是弱酸 |
| D、若1<a<4,则A、B、C都是弱酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com