
| A. | 液氯、晶体硅、臭氧均属于单质 | B. | 盐酸、醋酸、苯酚均属于强电解质 | ||
| C. | CO2、CCl4、蛋白质均属于有机物 | D. | CuO、MgO、Na2O2均属于碱性氧化物 |
分析 A.单质是由同种元素的原子组成的纯净物;
B.水溶液中能完全电离的电解质为强电解质;
C.有机物是指含有碳元素的化合物.无机物是指不含有碳元素的化合物.一氧化碳、二氧化碳、碳酸盐等物质中虽然含有碳元素,但是这些物质的性质和无机物相似,把它们归入无机物;
D.碱性氧化物是指能与酸反应生成盐和水的金属氧化物.
解答 解:A.液氯、晶体硅、臭氧均是由同种元素的原子组成的纯净物,属于单质,故A正确;
B.醋酸和苯酚在水溶液中部分电离,属于弱电解质,故B错误;
C.CO2属于无机物,故C错误;
D.因过氧化钠与酸反应生成盐、水和氧气,则过氧化钠不属于碱性氧化物,故D错误.
故选A.
点评 本题考查物质的分类,明确相关的概念是解答本题的关键,题目难度不大.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:解答题
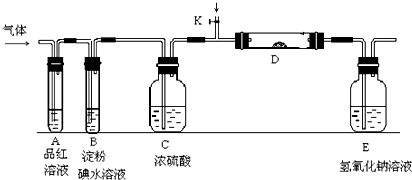
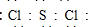 ,Y2W2的结构式为Cl-S-S-Cl.
,Y2W2的结构式为Cl-S-S-Cl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B、C的分子数之比为1:3:2 | |
| B. | A、B、C的浓度相等 | |
| C. | 单位时间生成 nmol A,同时生成 3nmol B | |
| D. | 生成C的速率与C分解的速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的电负性大于Y的电负性 | B. | X的原子半径大于Y的原子半径 | ||
| C. | X的氧化性大于Y的氧化性 | D. | X的第一电离能大于Y的第二电离能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
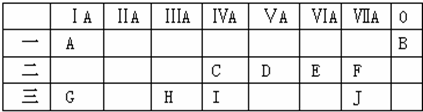
 ,元素H与元素J组成的化合物的水溶液中加入少量烧碱溶液,反应的离子方程式为Al3++3OH-=Al(OH)3↓.
,元素H与元素J组成的化合物的水溶液中加入少量烧碱溶液,反应的离子方程式为Al3++3OH-=Al(OH)3↓.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极反应:H2-2e-═2 H+ | |
| B. | 通O2的一极是发生还原反应 | |
| C. | 工作一段时间后电解质溶液的c(OH-)增大 | |
| D. | 工作时负极区附近pH增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com