
【题目】下列离子方程式书写正确的是( )
A.铝粉投入到NaOH溶液中:2Al+2OH-= 2AlO2-+H2↑
B.铁和稀硝酸反应: Fe+2H+=Fe2++H2↑
C.AlCl3溶液中加入足量的氨水:Al3++ 3OH- = Al(OH)3↓
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2 = 2Fe3++2Cl-
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】碳酸二甲酯[(CH3O)2CO]是一种具有发展前景的“绿色”化工产品,电化学合成碳酸二甲酯的工作原理如图所示(加入两极的物质均是常温常压下的物质)。下列说法正确的是
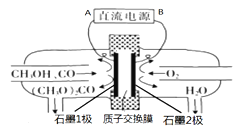
A. B为直流电源正极
B. H+由石墨2极通过质子交换膜向石墨l极移动
C. 石墨l极发生的电极反应为:2CH3OH + CO-2e= (CH3O)2CO + 2H+
D. 电解一段时间后,阴极和阳极消耗的气体的物质的量之比为l∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应的实验装置如图。下列有关铝热反应的说法中,不正确的是
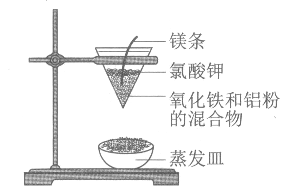
A. 铝热反应是放热反应
B. 铝热反应可用于冶炼某些高熔点金属
C. 实验中镁条的主要作用是还原氧化铁
D. 实验现象为火星四溅,漏斗下方有红热熔融物流出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中常伴随着能量变化。将Al条打磨后,插入6 mol/L盐酸中。
(1)Al与盐酸反应的离子方程式是________。
(2)该反应的能量变化可用下图中的________表示(填序号)。

(3)H2的产生速率随时间的变化如图所示。

t1~t2速率变化的主要原因是________。
t2~t3速率变化的主要原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在下列溶液中可能大量共存的离子组是
A. pH=0的溶液:Fe2+、Mg2+、NO3-、SO42-
B. 由水电离出的c(H+)=1×10-13 mol/L的溶液:Al3+、K+、SO42-、Cl-
C. c (OH-)/c(H+)=1012的溶液中:Na+、SO42-、NO3-、HCO3-
D. 滴加KSCN变红色的溶液:Na+、K+、Al3+、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属晶体判断正确的是
A.简单立方、配位数6、空间利用率68%
B.钾型、配位数6、空间利用率68%
C.镁型、配位数8、空间利用率74%
D.铜型、配位数12、空间利用率74%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E 都为短周期元素,A 原子失去一个电子后成为一个质子;C 的-1 价阴离子与氖原子具有相同的电子层结构;D在C 的下一周期,D可与同周期的B形成 BD2型离子化含物;E 和 C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题。
(1)B元素在元素周期表中的位置是____________。
(2)A与 E 形成的最简单化合物的电子式为____________。
(3)C的氢化物与 D的氢化物的沸点相比较: ____________(用化学式表示,且用>符号连接)。 解释原因______________。
(4)E 的氢化物与 E 的最高价氧化物对应水化物反应的生成物中含有的的化学键有____________。
(5)E 的最高价氧化物对应的水化物的稀溶液与过量铁粉发生反应的离子方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为原子序数依次增大的短周期主族元素,W、X处于不同周期,原子的最外层电子数X比Y多一个但比Z少一个,原子的电子层数X比Y、Z少一层。下列说法正确的是
A. 原子半径的大小为:Z>Y>X>W
B. 若Y、Z的核电荷数之和为X的4倍,则X、Z的气态氢化物的沸点:前者低于后者
C. 元素的非金属性:Y>Z
D. 若X的单质为常见的非金属导体,则Y的简单离子能破坏水的电离平衡
【答案】D
【解析】根据题意W是H元素;X、Y、Z在元素周期表的相对位置是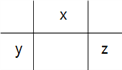 ;原子半径的大小为:Y>Z>X>W,故A错误;若Y、Z的核电荷数之和为X的4倍,则X、Z分别是O、Cl,的气态氢化物的沸点:H2O>HCl,故B错误;同周期元素从左到右非金属性增强,元素的非金属性:Y<Z,故C错误;若X的单质为常见的非金属导体,X是碳元素, Y是Al元素,Al3+水解促进水的电离,故D正确。
;原子半径的大小为:Y>Z>X>W,故A错误;若Y、Z的核电荷数之和为X的4倍,则X、Z分别是O、Cl,的气态氢化物的沸点:H2O>HCl,故B错误;同周期元素从左到右非金属性增强,元素的非金属性:Y<Z,故C错误;若X的单质为常见的非金属导体,X是碳元素, Y是Al元素,Al3+水解促进水的电离,故D正确。
【题型】单选题
【结束】
6
【题目】特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如右图,A极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。隔膜只允许特定的离子通过,电池反应式LixC6+Li1-xCoO2![]() C6+LiCoO2,下列说法不正确的是
C6+LiCoO2,下列说法不正确的是
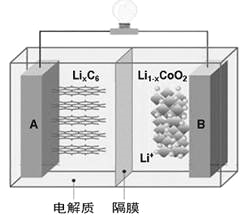
A. 据题意分析可知该隔膜只允许Li+通过,放电时Li+从左边移向右边
B. 放电时,正极锂的化合价未发生改变
C. 废旧钴酸锂电池进行“放电处理”让Li+进入石墨中而有利于回收
D. 充电时阳极的电极反应式为:LiCoO2-xe-=Li1-xCoO2+xLi+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的实验方法正确的是( )
A.除去CO2中少量O2:用点燃的方法
B.除去NaCl溶液中的Na2SO4:加入适量Ba(NO3)2溶液后,过滤
C.除去Cu中的少量Fe:加入足量稀硫酸溶液后,过滤,洗涤,干燥
D.除去CO2中的少量HCl:通入NaOH溶液后,收集气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com