
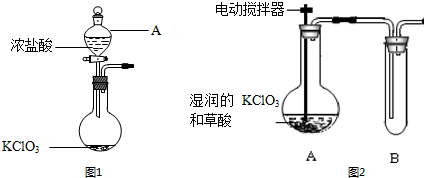

分析 (1)由仪器结构特征,可知A为分液漏斗;氯酸钾与浓盐酸反应生成氯气、氯化钾与水;
(2)①反应控制温度为60℃,应采取水浴加热;
②ClO2是一种黄绿色、有刺激性气味的气体,熔点:-59.0℃,沸点:11.0℃,B装置要放置在冰水中,冷凝便于收集;
③ClO2易与碱反应;
(3)ClO2与H2O2在氢氧化钠溶液中反应制得NaClO2,Cl元素化合价降低,则ClO2为氧化剂,H2O2为还原剂,过氧化氢中氧元素被氧化;
(4)可以测定相同浓度酸的pH或测定相同浓度亚氯酸钠和次氯酸钠溶液的pH.
解答 解:(1)由仪器结构特征,可知A为分液漏斗;氯酸钾与浓盐酸反应生成氯气、氯化钾与水,反应方程式为:KClO3+6HCl(浓)═3Cl2↑+KCl+3H2O,
故答案为:分液漏斗;KClO3+6HCl(浓)═3Cl2↑+KCl+3H2O;
(2)①反应控制温度为60℃,应采取水浴加热,故答案为:水浴加热;
②ClO2是一种黄绿色、有刺激性气味的气体,熔点:-59.0℃,沸点:11.0℃,B装置要放置在冰水中,使ClO2 冷凝,便于收集,故答案为:使ClO2 冷凝,便于收集;
③ClO2易与碱反应,可以用氢氧化钠溶液吸收,故选:B;
(3)ClO2与H2O2在氢氧化钠溶液中反应制得NaClO2,Cl元素化合价降低,则ClO2为氧化剂,H2O2为还原剂,过氧化氢中氧元素被氧化,氧化产物为,故答案为:O2;
(4)分别取等物质的量浓度的亚氯酸和次氯酸溶液于两个烧杯中,测其pH值,次氯酸溶液的pH比亚氯酸溶液的pH大,
故答案为:分别取等物质的量浓度的亚氯酸和次氯酸溶液于两个烧杯中,测其pH值;次氯酸溶液的pH比亚氯酸溶液的pH大.
点评 本题考查物质制备实验、对操作与装置的分析评价、氧化还原反应、实验方案设计等,是对基础知识的综合应用,注意对题目信息的应用,难度中等.


科目:高中化学 来源: 题型:选择题
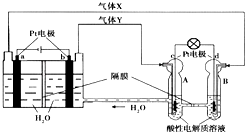 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )| A. | 当有0.1mol电子转移时,a极产生1.12L O2(标况) | |
| B. | b极上发生的电极反应是:2H++2e-═H2↑ | |
| C. | d极上发生的电极反应是:O2+4H++4e-═2H2O | |
| D. | c极上进行还原反应,B中的H+可以通过隔膜进入A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
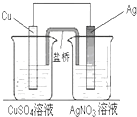 用铜片、银片、CuSO4溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是 ( )
用铜片、银片、CuSO4溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是 ( )| A. | ①② | B. | ③④ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性NaHCO3<Na2CO3 | B. | 常温时水中溶解度NaHCO3>Na2CO3: | ||
| C. | 与盐酸反应的速率:NaHCO3>Na2CO3 | D. | 相对分子质量:NaHCO3<Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化 (Q1,Q2,Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | a1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | a2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | a3 | c3 | 放出Q3kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
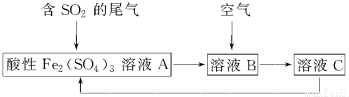
| A. | 溶液B中发生的反应为2SO2+O2═2SO3 | |
| B. | 可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+ | |
| C. | 由以上流程可推知氧化性:Fe3+>O2>SO42- | |
| D. | 此工艺的优点之一是物质能循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
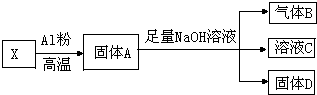 某同学设计实验将Fe3O4和CuO组成的混合物X进行如图所示的转化(每一步均反应完全)
某同学设计实验将Fe3O4和CuO组成的混合物X进行如图所示的转化(每一步均反应完全)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com