
| A. | 将金属A投入B的盐溶液,A溶解说明A的金属性比B的金属性强 | |
| B. | 氯碱工业和金属钠的冶炼都用到了NaC1,在电解时它们的阴极都是Na+得电子 | |
| C. | 向硫酸溶液中加入适量氨水,当溶液中c(SO42-)=c(NH4+)时,溶液呈酸性 | |
| D. | 等物质的量浓度的下列溶液中①NH4Cl ②NH4Al(SO4)2 ③NH3•H2O ④CH3COONH4,c(NH4+)由大到小的顺序是:①>②>③>④ |
分析 A.A溶解,不能说明A的金属性比B的金属性强,如铜与氯化铁的反应;
B.氯碱工业中阴极氢离子得到电子生成氢气,钠离子不会得到电子;
C.溶液为中性时2c(SO42-)=c(NH4+),根据混合液中的电荷守恒判断;
D.醋酸根离子促进了了铵根离子的水解,铝离子抑制了铵根离子的水解,一水合氨的电离程度较小,氨水中铵根离子浓度最小.
解答 解:A.将金属A投入B的盐溶液,A溶解,没有指出置换出B,则不能说明A的金属性比B的金属性强,如铜与氯化铁的反应,故A错误;
B.冶炼金属钠需要电解熔融氯化钠,阴极钠离子得到电子生成钠,而氯碱工业中氢离子得到电子生成氢气,钠离子不会得到电子,故B错误;
C.向硫酸溶液中加入适量氨水,当溶液中c(SO42-)=c(NH4+)时,根据电荷守恒可知:c(OH-)<c(H+)时,则混合液呈酸性,故C正确;
D.等物质的量浓度的①NH4Cl ②NH4Al(SO4)2 ③NH3•H2O ④CH3COONH4,②中铝离子抑制了铵根离子的水解,③中电离程度较小,其溶液中铵根离子浓度最小,④中醋酸钙离子促进了铵根离子的水解,则c(NH4+)由大到小的顺序是:②>①>④>③,故D错误;
故选C.
点评 本题考查了离子浓度大小比较,题目难度中等,涉及金属性强弱判断、盐的水解原理及其应用、电解原理等知识,注意掌握盐的水解原理,明确电荷守恒在判断离子浓度大小中的应用,试题培养了学生分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁胶体能吸附水中的悬浮颗粒并沉降,起到净水作用 | |
| B. | 胶体的分散质粒子的直径大于10-7m | |
| C. | 当光束通过硫酸铜溶液时可看见一条光亮的通路 | |
| D. | 胶体和溶液、浊液的本质区别是能否产生“丁达尔效应” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠在医疗上是治疗胃酸过多的一种药剂 | |
| B. | 盐酸、漂白粉属于混合物,而液氯、水玻璃均属于纯净物 | |
| C. | 玻璃、水泥、水晶项链都是硅酸盐制品 | |
| D. | 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol/L盐酸 | B. | pH=11氨水 | ||
| C. | pH=4NaHSO3溶液 | D. | 0.01mol/L Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
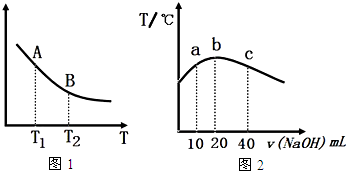 碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题:
碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚钠溶液中通少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| B. | 向Ca(ClO)2溶液中通入过量SO2:Ca2++2ClO-+SO2+H2O═CaSO4↓+2H++Cl-+HClO | |
| C. | 用新制的氢氧化铜悬浊液检验乙醛中的醛基:CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+Cu2O↓+3H2O | |
| D. | 在碳酸氢钙溶液中加入过量的氢氧化钙溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2→H2CO3 | B. | Al(OH)3→Al2O3 | C. | Na2O2→Na2CO3 | D. | SiO2→H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com