
| A. | 配制过程只需要三种仪器即可完成 | |
| B. | 容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液物质的量浓度为3.99mol/L | |
| D. | 需要称量的NaClO固体的质量为140g |
分析 A.配制过程中需要用到天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管等;
B.容量瓶中有水,对溶液的体积无影响;
C.根据含25%NaClO、密度1.19g•cm-3,及根据c=$\frac{1000ρw}{M}$来计算;
D.容量瓶的规格没有480mL,应选取500 mL的容量瓶进行配制.
解答 解:A.需用托盘天平、药匙称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量瓶和胶头滴管来定容,故A错误;
B.容量瓶中有水,对溶液的体积无影响,所以经洗涤干净的容量瓶不必烘干后再使用,故B错误;
C.由c=$\frac{1000ρw}{M}$,则c(NaClO)=$\frac{1000mL×1.19g•c{m}^{-3}×25%}{74.5g•mo{l}^{-1}}$=3.99mol•L-1,故C正确;
D.应选取500 mL的容量瓶进行配制,然后取出480mL即可,所以需要NaClO的质量:500mL×1.19 g•cm-3×25%=148.75g,应该用托盘天平称量148.8g次氯酸钠,故D错误;
故选C.
点评 本题主要溶液配制的步骤、仪器以及误差分析等知识,题目难度中等,注意注意配制一定浓度的溶液方法,D为易错点,需要明确计算溶质的质量时,溶液的体积按500mL计算.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 48gO3含有6.02×1023个氧原子 | |
| B. | 常温常压下,11.2L甲烷气体含有3.01×1023个甲烷分子 | |
| C. | 1L0.1mol•L-1MgCl2溶液中含有2×6.02×1023个离子 | |
| D. | 0.1molNH4+离子含有6.02×1023个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe+Cl2 (过量)→ | B. | Fe+浓盐酸(过量)→ | C. | FeBr2(过量)+Cl2→ | D. | FeCl3+Fe(少量)→ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
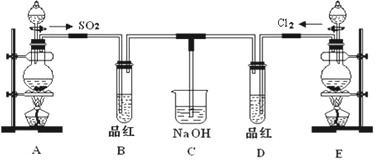
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜和硝酸反应 | B. | 二氧化碳通入氢氧化钠溶液中 | ||
| C. | 细铁丝在氯气中燃烧 | D. | 铁和与硫酸溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为8的碳原子:${\;}_{6}^{8}$C | B. | 氯化钙的电子式: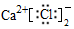 | ||
| C. | S2-的结构示意图: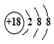 | D. | 2-溴丙烷的结构简式:(CH3)2CHBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 残余固体可能为铁和铜的混合物 | |
| B. | 最后得到的溶液可能含有Fe3+ | |
| C. | 残余固体是铁,溶液中一定不含Cu2+ | |
| D. | 残余固体一定全部是铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1 mol•L-1 NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合:$\frac{3}{2}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1 Na2C2O4溶液与0.1 mol•L-1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com