
”¾ĢāÄæ”æČēĶ¼ŹĒ²æ·Ö¶ĢÖÜĘŚŌŖĖŲ»ÆŗĻ¼ŪÓėŌ×ÓŠņŹżµÄ¹ŲĻµĶ¼£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A. Ąė×Ó°ė¾¶£ŗX£¾Y£¾Z
B. WX3ŗĶĖ®·“Ó¦ŠĪ³ÉµÄ»ÆŗĻĪļŹĒĄė×Ó»ÆŗĻĪļ
C. ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌ£ŗR£¾W
D. YŗĶZĮ½Õß×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÄÜĻą»„·“Ó¦
”¾“š°ø”æB
”¾½āĪö”æ
XÓŠ-2¼Ū£¬ĪŖŃõŌŖĖŲ£¬YĪŖ+1¼Ū£¬ĪŖÄĘ£¬ZĪŖ+3¼Ū£¬ĪŖĀĮ£¬WĪŖ+6¼Ū£¬ĪŖĮņ£¬RĪŖ+7¼Ū£¬ĪŖĀČ”£Ōņ
A”¢ŃõĄė×Ó”¢ÄĘĄė×ÓŗĶĀĮĄė×Óµē×Ó²ć½į¹¹ĻąĶ¬£¬ŗĖµēŗÉŹżŌ½“󣬰ė¾¶Ō½Š”£¬Ąė×Ó°ė¾¶£ŗX£¾Y£¾Z£¬AÕżČ·£»
B”¢ČżŃõ»ÆĮņČÜÓŚĖ®Éś³ÉĮņĖį£¬ŹōÓŚŗ¬ÓŠ¹²¼Ū¼üµÄ¹²¼Ū»ÆŗĻĪļ£¬B“ķĪó£»
C”¢Ķ¬ÖÜĘŚŌŖĖŲ£¬“Ó×óµ½ÓŅ£¬·Ē½šŹōŠŌŌöĒ棬×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄĖįŠŌŌöĒ棬¹Ź×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌ£ŗR£¾W£¬CÕżČ·£»
D”¢YŗĶZĮ½Õß×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÄÜĻą»„·“Ó¦£¬¼“ĒāŃõ»ÆÄĘŗĶĒāŃõ»ÆĀĮ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬DÕżČ·”£
“š°øŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲČČ»Æѧ·½³ĢŹ½ŹéŠ“¼°¶ŌÓ¦±ķŹö¾łÕżČ·µÄŹĒ
A. ÅØH2SO4Óė0.1 mol”¤L£1NaOH·“Ó¦£ŗH£«(aq)£«OH£(aq)===H2O(l) ¦¤H£½£57.3 kJ”¤mol£1
B. ĆܱÕČŻĘ÷ÖŠ£¬9.6 gĮņ·ŪÓė11.2 gĢś·Ū»ģŗĻ¼ÓČČ³ä·Ö·“Ó¦£¬·Å³ö19.12 kJČČĮ攣ŌņFe(s)£«S(s)===FeS(s)””¦¤H£½£95.6 kJ”¤mol£1
C. ŅŃÖŖ1 molĒāĘųĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®Ėł·Å³öµÄČČĮæĪŖ285.5 kJ£¬ŌņĖ®·Ö½āµÄČČ»Æѧ·½³ĢŹ½£ŗ2H2O(l)===2H2(g)£«O2(g)””¦¤H£½£«285.5 kJ”¤mol£1
D. ŅŃÖŖ2C(s)£«O2(g)===2CO(g)””¦¤H£½£221 kJ”¤mol£1£¬ŌņæÉÖŖCµÄČ¼ÉÕČȦ¤H£½£110.5 kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ¹ŲÄÜĮæµÄÅŠ¶Ļ»ņ±ķŹ¾·½·ØÕżČ·µÄŹĒ£Ø””””£©
A. ŠčŅŖ¼ÓČČ²ÅÄÜ·¢ÉśµÄ·“Ó¦Ņ»¶ØŹĒĪüČČ·“Ó¦
B. “ÓC(ŹÆÄ«£¬![]() ½šøÕŹÆ£¬
½šøÕŹÆ£¬![]()
![]() £¬æÉÖŖ£ŗ½šøÕŹÆ±ČŹÆÄ«øüĪȶØ
£¬æÉÖŖ£ŗ½šøÕŹÆ±ČŹÆÄ«øüĪȶØ
C. µČÖŹĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬Ē°Õ߷ųöČČĮæøü¶ą
D. Čō![]()
![]() £¬Ōņ
£¬Ōņ![]() Č¼ÉÕČČĪŖ
Č¼ÉÕČČĪŖ![]()
![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻÓĆÖŲøõĖįÄĘ(Na2Cr2O7)½į¾§ŗóµÄÄøŅŗ(ŗ¬ÉŁĮæŌÓÖŹFe3+)Éś²śÖŲøõĖį¼Ų (K2Cr2O7)£¬Ę乤ŅÕĮ÷³Ģ¼°Ļą¹ŲĪļÖŹČܽā¶ČĒśĻßČēĻĀĶ¼ĖłŹ¾”£
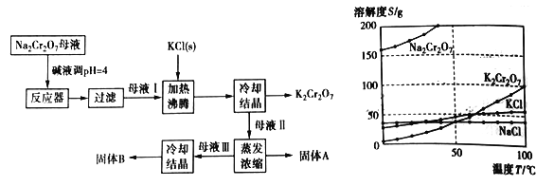
£Ø1£©ĻņNa2Cr2O7ÄøŅŗÖŠ¼Ó¼īŅŗµ÷pHµÄÄæµÄŹĒ_____________________”£
£Ø2£©ĶعżĄäČ“½į¾§Īö³ö“óĮæK2Cr2O7µÄŌŅņŹĒ________________________________”£
£Ø3£©¹ĢĢåAµÄÖ÷ŅŖ³É·ÖĪŖ__________£ØĢī»ÆѧŹ½£©£¬ÓĆČČĖ®Ļ“µÓ¹ĢĢåA£¬»ŲŹÕµÄĻ“µÓŅŗ×ŖŅʵ½ÄøŅŗ___________(Ģī”°I”±”°¢ņ”±»ņ”°¢ó”±)ÖŠ£¬¼ČÄÜĢįøß²śĀŹÓÖæÉŹ¹ÄÜŗĽµµĶ”£¹ĢĢåBµÄÖ÷ŅŖ³É·ÖĪŖ___________________£ØĢī»ÆѧŹ½£©”£
£Ø4£©²ā¶Ø²śĘ·ÖŠK2Cr2O7ŗ¬ĮæµÄ·½·ØČēĻĀ£ŗ³ĘČ”²śĘ·ŹŌŃł2.500 g Åä³É250 mLČÜŅŗ£¬ÓĆŅĘŅŗ¹ÜČ”³ö25.00 mLÓŚµāĮæĘæÖŠ£¬¼ÓČė10 mL 2 mol”¤L-l H2SO4ČÜŅŗŗĶ×ćĮæKIČÜŅŗ(øõµÄ»¹Ō²śĪļĪŖCr3+)£¬·ÅÖĆÓŚ°µ“¦5 min£¬Č»ŗó¼ÓČė100 mLÕōĮóĖ®”¢3 mL µķ·ŪÖøŹ¾¼Į£¬ÓĆ0.1200 mol”¤L-l Na2S2O3±ź×¼ČÜŅŗµĪ¶Ø(ŅŃÖŖI2+ 2S2O32-=2I-+S4O62-)”£
¢ŁĖįŠŌČÜŅŗÖŠKI ÓėK2Cr2O7·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____________________________”£
¢ŚČōŹµŃéÖŠ¹²ÓĆČ„Na2S2O3±ź×¼ČÜŅŗ40.00 mL£¬ŌņĖłµĆ²śĘ·ÖŠÖŲøõĖį¼ŲµÄ“æ¶ČĪŖ__________%( ±£Įō2 Ī»Š”Źż£¬ÉčÕūøö¹ż³ĢÖŠĘäĖūŌÓÖŹ²»²ĪÓė·“Ó¦)”£½ųŅ»²½Ģį“æ²śĘ·µÄ·½·ØŹĒ___________________”£
£Ø5£©+6¼ŪCrµÄ¶¾ŠŌŗÜøߣ¬¹¤ŅµÉĻÓƵē½ā·ØĄ““¦Ąķŗ¬Cr2O72-µÄ·ĻĖ®”£ĻĀĶ¼ĪŖµē½ā×°ÖĆŹ¾ŅāĶ¼£¬µē¼«²ÄĮĻ·Ö±šĪŖĢśŗĶŹÆÄ«”£Ķصēŗó£¬Cr2O72-ŌŚb¼«ø½½ü×Ŗ±äĪŖCr3+£¬Ņ»¶ĪŹ±¼äŗóCr3+×īÖÕæÉŌŚa ¼«ø½½ü±ä³ÉCr(OH)3³Įµķ¶ų±»³żČ„”£

¢ŁŌŚŅŌÉĻ“¦Ąķ¹ż³ĢÖŠ£¬Cr2O72-×Ŗ»ÆĪŖ¶¾ŠŌ½ĻµĶµÄCr3+µÄĄė×Ó·½³ĢŹ½ĪŖ________________________”£
¢Śaµē¼«µÄµē¼«·“Ó¦Ź½ŹĒŹĒ____________________£»µē½āŅ»¶ĪŹ±¼äŗóŌŚŅõ¼«ĒųÓŠFe(OH)3ŗĶGr(OH)3³ĮµķÉś³É£¬Čōµē½āŗóµÄČÜŅŗÖŠc(Cr3+)ĪŖ3”Į10-5mol”¤L-1£¬ŌņČÜŅŗÖŠc(Fe3+)ĪŖ____________ mol”¤L-1”£ŅŃÖŖ£ŗKsp=[Fe(OH)3]=4.0”Į10-38£¬K[Cr(OH)3]=6.0”Į10-31”£
”¾“š°ø”æ ³żČ„Fe3+ µĶĪĀĻĀK2Cr2O7µÄČܽā¶ČŌ¶Š”ÓŚĘäĖū×é·Ö£¬ĒŅĖęĪĀ¶ČµÄ½µµĶ£¬K2Cr2O7µÄČܽā¶ČĆ÷ĻŌ¼õŠ” NaCl ¢ņ K2Cr2O7 Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O 94.08 ÖŲ½į¾§ Cr2O72-+6Fe2++ 14H+=2Cr3++6Fe3++7H2O 2H++2e-=H2”ü 2”Į10-12
”¾½āĪö”ææ¼²é»Æѧ¹¤ŅÕĮ÷³Ģ£¬£Ø1£©øł¾ŻĢāÄæŠÅĻ¢£¬ÄøŅŗÖŠŗ¬ÓŠÉŁĮæµÄFe3£«£¬¼Ó¼īŅŗµÄÄæµÄŹĒ³żČ„Fe3£«£»£Ø2£©øł¾ŻĪĀ¶ČÓėČܽā¶ČµÄ¹ŲĻµ£¬K2Cr2O7µÄČܽā¶ČŹÜĪĀ¶ČµÄÓ°Ļģ½Ļ“󣬵ĶĪĀŹ±K2Cr2O7µÄČܽā¶ČŌ¶Š”ÓŚĘäĖū×é·Ö£¬ĒŅĪĀ¶Č½µµĶ£¬K2Cr2O7µÄČܽā¶ČŹÜĪĀ¶ČµÄÓ°Ļģ½Ļ“󣻣Ø3£©ÄøŅŗIÖŠ¼ÓČėKCl£¬·¢ÉśNa2Cr2O7£«KCl=K2Cr2O7£«NaCl£¬²ÉÓĆĄäČ“½µĪĀµĆµ½K2Cr2O7¹ĢĢ壬¼“ÄøŅŗIIÖŠŗ¬ÓŠ“óĮæµÄNaCl£¬Ņņ“ĖÕō·¢ÅØĖõµĆµ½µÄ¹ĢĢåŹĒNaCl£»ĄäČ“½į¾§ÖŠÓŠ“óĮæµÄK2Cr2O7Īö³ö£¬µ«ČÜŅŗÖŠŗ¬ÓŠÉŁĮæµÄK2Cr2O7£¬Õō·¢ÅØĖõŹ±£¬NaCl±ķĆęø½×ÅŅ»²æ·ÖK2Cr2O7£¬ĪŖĮĖĢįøß²śĀŹÓÖæÉŹ¹ÄÜŗĽµµĶ£¬Ņņ“ĖŠčŅŖ°ŃĻ“µÓŅŗ×ŖŅʵ½ÄøŅŗIIÖŠ£¬“ļµ½ĄąĖĘø»¼ÆµÄÄæµÄ£»Ņņ“Ė¹ĢĢåBµÄÖ÷ŅŖ³É·ÖŹĒK2Cr2O7£»£Ø4£©¢Łøł¾Ż²Ł×÷£¬µĆ³öK2Cr2O7×÷Ńõ»Æ¼Į£¬±¾Éķ±»»¹Ō³ÉCr3£«£¬I£±»Ńõ»Æ³ÉI2£¬Ņņ“ĖÓŠCr2O72££«I£”śCr3£«£«I2£¬Č»ŗó²ÉÓĆ»ÆŗĻ¼ŪÉż½µ·Ø”¢Ō×ÓŹŲŗćÅäĘ½¼“æÉ£¬Ąė×Ó·½³ĢŹ½ĪŖCr2O72£+6I£+14H£«=2Cr3£«+3I2+7H2O£»¢Śøł¾ŻĄė×Ó·½³ĢŹ½£¬µĆ³ö¹ŲĻµŹ½ĪŖCr2O72£”«3I2”«6S2O32££¬ŌņĒó³öѳʷ֊K2Cr2O7µÄÖŹĮæĪŖ =2.352g£¬“æ¶ČĪŖ2.352/2.500”Į100%=94.08%£»½ųŅ»²½Ģį“æŠčŅŖÖŲŠĀČܽā£¬ĄäČ“½į¾§£¬“Ė·½·Ø½ŠÖŲ½į¾§£»£Ø5£©¢Łbµē¼«ĪŖŃō¼«£¬Ó¦ŹĒŹ§Č„µē×Ó£¬»ÆŗĻ¼ŪӦɿøߣ¬¶ųCr2O72£ÖŠCrµÄ»ÆŗĻ¼Ū½µµĶ£¬Ņņ“Ėbµē¼«ĪŖĢś£¬“Ėµē¼«·“Ó¦Ź½ĪŖFe£2e£=Fe2£«£¬Č»ŗóĄūÓĆCr2O72£µÄŃõ»ÆŠŌ£¬ÓėFe2£«·¢Éś·“Ó¦£¬Ąė×Ó·“Ó¦·½³Ģ·½Ź½ĪŖCr2O72£+6Fe2£«+ 14H£«=2Cr3£«+6Fe3£«+7H2O£»¢Śøł¾Ż¢ŁµÄ·ÖĪö£¬aµē¼«ĪŖŅõ¼«£¬µē¼«·“Ó¦Ź½ĪŖ2H£«£«2e£=H2”ü£»Cr3£«ŗĶFe3£«¹²“ęŌŚĶ¬Ņ»ČÜŅŗÖŠ£¬Ņņ“ĖÓŠ
=2.352g£¬“æ¶ČĪŖ2.352/2.500”Į100%=94.08%£»½ųŅ»²½Ģį“æŠčŅŖÖŲŠĀČܽā£¬ĄäČ“½į¾§£¬“Ė·½·Ø½ŠÖŲ½į¾§£»£Ø5£©¢Łbµē¼«ĪŖŃō¼«£¬Ó¦ŹĒŹ§Č„µē×Ó£¬»ÆŗĻ¼ŪӦɿøߣ¬¶ųCr2O72£ÖŠCrµÄ»ÆŗĻ¼Ū½µµĶ£¬Ņņ“Ėbµē¼«ĪŖĢś£¬“Ėµē¼«·“Ó¦Ź½ĪŖFe£2e£=Fe2£«£¬Č»ŗóĄūÓĆCr2O72£µÄŃõ»ÆŠŌ£¬ÓėFe2£«·¢Éś·“Ó¦£¬Ąė×Ó·“Ó¦·½³Ģ·½Ź½ĪŖCr2O72£+6Fe2£«+ 14H£«=2Cr3£«+6Fe3£«+7H2O£»¢Śøł¾Ż¢ŁµÄ·ÖĪö£¬aµē¼«ĪŖŅõ¼«£¬µē¼«·“Ó¦Ź½ĪŖ2H£«£«2e£=H2”ü£»Cr3£«ŗĶFe3£«¹²“ęŌŚĶ¬Ņ»ČÜŅŗÖŠ£¬Ņņ“ĖÓŠ £¬½āµĆc(Fe3£«)=2.0”Į10£12mol”¤L£1”£
£¬½āµĆc(Fe3£«)=2.0”Į10£12mol”¤L£1”£
µć¾¦£ŗŃõ»Æ»¹Ō·“Ó¦·½³ĢŹ½µÄŹéŠ“ŹĒѧɜµÄŅ»øöÄŃµć£¬Ń§ÉśĶłĶłÕŅ²»³ö·“Ó¦Īļ»ņÉś³ÉĪļ£¬»ņÕßČÜŅŗµÄ»·¾³Ń”“ķ£¬ÕāŹĒ¶ŌĢāµÄĄķ½āÉĻ²»Ķø³¹£¬Čē±¾ĢāµÄ(5)¢Łøł¾ŻŠÅĻ¢£¬Cr2O72£ŌŚb¼«ø½½ü×Ŗ±äĪŖCr3£«£¬b¼«ĪŖŃō¼«£¬Ńō¼«ÉĻŹ§Č„µē×Ó»ÆŗĻ¼ŪÉżøߣ¬¶ųĻÖŌŚCrµÄ»ÆŗĻ¼Ū½µµĶ£¬Ņņ“ĖÖ»ÄÜĖµĆ÷b¼«µÄ²ÄĮĻŹĒFe£¬Fe£2e£=Fe2£«£¬Č»ŗó»¹ŌCr2O7££¬Ņņ“ĖÓŠCr2O72££«Fe2£«”śFe3£«£«Cr3£«£¬øł¾Ż»ÆŗĻ¼ŪÉż½µ·Ø½ųŠŠÅäĘ½£¬¼“Cr2O72££«6Fe2£«”ś2Cr3£«£«6Fe3£«£¬Fe2£«”¢Fe3£«”¢Cr3£«²»ÓėOH£“óĮæ¹²“ę£¬Ņņ“ĖČÜŅŗĻŌĖįŠŌ£¬øł¾Ż·“Ó¦Ē°ŗóĖł“ųµēŗÉŹżŹŲŗć”¢Ō×ÓŹŲŗć½ųŠŠÅäĘ½¼“æÉ”£
”¾ĢāŠĶ”æ×ŪŗĻĢā
”¾½įŹų”æ
10
”¾ĢāÄæ”æ”°µĶĢ¼¾¼Ć”±Õż³ÉĪŖæĘѧ¼ŅŃŠ¾æµÄÖ÷ŅŖæĪĢā£¬ĪŖĮĖ¼õÉŁæÕĘųÖŠµÄĪĀŹŅĘųĢ壬²¢ĒŅ³ä·ÖĄūÓƶžŃõ»ÆĢ¼×ŹŌ“£¬æĘѧ¼ŅĆĒÉčĻėĮĖŅ»ĻµĮŠ²¶×½ŗĶ·ā“궞Ńõ»ÆĢ¼µÄ·½·Ø”£
£Ø1£©ÓŠæĘѧ¼ŅĢį³öæÉĄūÓĆFeOĪüŹÕŗĶĄūÓĆCO2£¬Ļą¹ŲČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ¦¤H=-76.0 kJ”¤mol-1
¢ŁÉĻŹö·“Ó¦ÖŠĆæÉś³É1 mol Fe3O4£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ_______mol”£
¢ŚŅŃÖŖ£ŗC(s)+2H2O(g)=CO2(g)+2H2(g) ”÷H=+113.4kJ”¤mol-1£¬Ōņ·“Ó¦£ŗ3FeO(s)+ H2O(g)= Fe3O4(s)+ H2(g)µÄ”÷H=__________”£
£Ø2£©ÓĆ°±Ė®²¶¼ÆŃĢĘųÖŠµÄCO2Éś³Éļ§ŃĪŹĒ¼õÉŁCO2ÅŷŵÄæÉŠŠ“ėŹ©Ö®Ņ»”£
¢Ł·Ö±šÓĆ²»Ķ¬pHµÄĪüŹÕ¼ĮĪüŹÕŃĢĘųÖŠµÄCO2£¬CO2ĶŃ³żŠ§ĀŹÓėĪüŹÕ¼ĮµÄpH¹ŲĻµČēĶ¼ĖłŹ¾£¬ČōŃĢĘųÖŠCO2µÄŗ¬Įæ£ØĢå»ż·ÖŹż£©ĪŖ12£„£¬ŃĢĘųĶØČė°±Ė®µÄĮ÷ĮæĪŖ0.052 m3”¤h-1(±ź×¼×“æö)£¬ÓĆpHĪŖ12.81µÄ°±Ė®ĪüŹÕŃĢĘų30min£¬ĶŃ³żµÄCO2µÄĪļÖŹµÄĮæ×ī¶ąĪŖ____________(¾«Č·µ½0.01)”£

¢ŚĶس£ĒéæöĻĀĪĀ¶ČÉżøߣ¬CO2ĶŃ³żŠ§ĀŹĢįøߣ¬µ«øßÓŚ40”ꏱ£¬ĶŃ³żCO2Š§ĀŹ½µµĶµÄÖ÷ŅŖŌŅņŹĒ______________”£
£Ø3£©Ņ»¶ØĢõ¼žĻĀ£¬Pd-Mg/SiO2“߻ƼĮæÉŹ¹CO2”°¼×Ķé»Æ”±“Ó¶ų±ä·ĻĪŖ±¦£¬Ęä·“Ó¦»śĄķČēĶ¼ĖłŹ¾”£

¢ŁøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ______________________£»·“Ó¦¹ż³ĢÖŠĢ¼ŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ-2¼ŪµÄÖŠ¼äĢåŹĒ_________________”£
¢ŚĻņŅ»ČŻ»żĪŖ2 LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ³äČėŅ»¶ØĮæµÄCO2ŗĶH2£¬ŌŚ300”ꏱ·¢ÉśÉĻŹö·“Ó¦£¬“ļµ½Ę½ŗāŹ±ø÷ĪļÖŹµÄÅØ¶Č·Ö±šĪŖCO2£ŗ0.2 mol”¤L-1”¢H2£ŗ0.8 mol”¤L-1”¢CH4£ŗ0.8 mol”¤L-1”¢H2O£ŗ1.6 mol”¤L-1£¬CO2µÄĘ½ŗā×Ŗ»ÆĀŹĪŖ_________________£»300”ꏱÉĻŹö·“Ó¦µÄĘ½ŗā³£ŹżK=___________________”£
¢ŪŅŃÖŖøĆ·“Ó¦Õż·“Ó¦·ÅČČ£¬ĻÖÓŠĮ½øöĻąĶ¬µÄŗćČŻ¾ųČČ(ÓėĶā½ēĪŽČČĮæ½»»»)ĆܱÕČŻĘ÷¢ń”¢¢ņ£¬ŌŚ¢ńÖŠ³äČė1molCO2ŗĶ4molH2£¬ŌŚ¢ņÖŠ³äČė1molCH4ŗĶ2molH2O(g)£¬300”ęĻĀæŖŹ¼·“Ó¦”£“ļµ½Ę½ŗāŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A.ČŻĘ÷¢ń”¢¢ņÖŠÕż·“Ó¦ĖŁĀŹĻąĶ¬
B.ČŻĘ÷¢ń”¢¢ņÖŠCH4µÄĪļÖŹµÄĮæ·ÖŹżĻąĶ¬
C.ČŻĘ÷¢ńÖŠCO2µÄĪļÖŹµÄĮæ±ČČŻĘ÷¢ņÖŠµÄ¶ą
D.ČŻĘ÷¢ńÖŠCO2µÄ×Ŗ»ÆĀŹÓėČŻĘ÷¢ņÖŠCH4µÄ×Ŗ»ÆĀŹÖ®ŗĶŠ”ÓŚ1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆĒāĘų¶Ō·ĻĘų½ųŠŠĶŃĢ¼“¦ĄķæÉŹµĻÖĀĢÉ«»·±£”¢·ĻĪļĄūÓĆ£¬¶ŌÓŚ¼õÉŁĪķö²Ņ²¾ßÓŠÖŲŅŖŅāŅ唣
£Ø1£©Ęū³µĪ²ĘųµÄÖ÷ŅŖĪŪČ¾ĪļĪŖNO£¬ÓĆH2“߻ƻ¹ŌNOæÉŅŌ“ļµ½Ļū³żĪŪČ¾µÄÄæµÄ”£
ŅŃÖŖ£ŗ2NO(g) ![]() N2(g)£«O2(g) ¦¤H=£180.5 kJ”¤mol£1
N2(g)£«O2(g) ¦¤H=£180.5 kJ”¤mol£1
2H2O(l)===2H2(g)£«O2(g) ¦¤H=£«571.6 kJ”¤mol£1
Š“³öH2(g)ÓėNO(g)·“Ӧɜ³ÉN2(g)ŗĶH2O(l)µÄČČ»Æѧ·½³ĢŹ½ŹĒ______________”£
£Ø2£©Ä³ŃŠ¾æŠ”×éÄ£ÄāŃŠ¾æČēĻĀ£ŗĻņ2 LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė2 mol NO·¢Éś·“Ó¦2NO(g) ![]() N2(g)£«O2(g)£¬ŌŚ²»Ķ¬µÄĪĀ¶ČĻĀ£¬·“Ó¦¹ż³ĢÖŠĪļÖŹµÄĮæÓėŹ±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
N2(g)£«O2(g)£¬ŌŚ²»Ķ¬µÄĪĀ¶ČĻĀ£¬·“Ó¦¹ż³ĢÖŠĪļÖŹµÄĮæÓėŹ±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ

¢ŁT2ĻĀ£¬ŌŚ0”«5 minÄŚ£¬v(O2)=______________mol”¤L£1”¤min£1£»øĆĪĀ¶ČĻĀ·“Ó¦N2(g)£«O2(g) ![]() 2NO(g)µÄĘ½ŗā³£ŹżK=______________”£
2NO(g)µÄĘ½ŗā³£ŹżK=______________”£
¢ŚøĆ·“Ó¦½ųŠŠµ½Mµć·Å³öµÄČČĮæ______________½ųŠŠµ½Wµć·Å³öµÄČČĮæ(Ģī”°£¾”±”¢”°£¼”±»ņ”°=”±)”£
MµćŹ±ŌŁ¼ÓČėŅ»¶ØĮæNO£¬Ę½ŗāŗóNOµÄ×Ŗ»ÆĀŹ______________(Ģī”°±ä“ó”±”¢”°±äŠ””±»ņ”°²»±ä”±)”£
¢Ū·“Ó¦æŖŹ¼ÖĮ“ļµ½Ę½ŗāµÄ¹ż³ĢÖŠ£¬ČŻĘ÷ÖŠĻĀĮŠø÷Ļī·¢Éś±ä»ÆµÄŹĒ______________(ĢīŠņŗÅ)”£
a£®»ģŗĻĘųĢåµÄĆÜ¶Č b£®Äę·“Ó¦ĖŁĀŹ
c£®µ„Ī»Ź±¼äÄŚ£¬N2ŗĶNOµÄĻūŗÄĮæÖ®±Č d£®ĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ
£Ø3£©ĒāĘų×÷ĪŖŅ»ÖÖĄķĻėČ¼ĮĻ£¬µ«²»ĄūÓŚÖü“ęŗĶŌĖŹä”£ĄūÓĆĒāÄÜŠčŅŖŃ”ŌńŗĻŹŹµÄ“¢Ēā²ÄĮĻ£¬ļēÄųŗĻ½šŌŚŅ»¶ØĢõ¼žĻĀæÉĪüŹÕĒāĘųŠĪ³ÉĒā»ÆĪļ£ŗLaNi5(s)£«3H2(g) ![]() LaNi5H6(s) ¦¤H£¼0£¬ÓūŹ¹LaNi5H6(s)ŹĶ·Å³öĘųĢ¬Ēā£¬øł¾ŻĘ½ŗāŅʶÆŌĄķ£¬æÉøıäµÄĢõ¼žŹĒ______________(Ģī×ÖÄø±ąŗÅ)”£
LaNi5H6(s) ¦¤H£¼0£¬ÓūŹ¹LaNi5H6(s)ŹĶ·Å³öĘųĢ¬Ēā£¬øł¾ŻĘ½ŗāŅʶÆŌĄķ£¬æÉøıäµÄĢõ¼žŹĒ______________(Ģī×ÖÄø±ąŗÅ)”£
A£®Ōö¼ÓLaNi5H6(s)µÄĮæ B£®ÉżøßĪĀ¶Č
C£®Ź¹ÓĆ“ß»Æ¼Į D£®¼õŠ”Ń¹Ēæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅĖįŅŅõ„ŹĒÖĘŅ©¹¤ŅµŗĶÓŠ»śŗĻ³ÉÖŠµÄÖŲŅŖŌĮĻ£¬ŹµŃéŹŅÖʱøŅŅĖįŅŅõ„µÄŹµŃé×°ÖĆ![]() ¼Š³Ö¼°¼ÓČČ×°ÖĆŅŃĀŌČ„
¼Š³Ö¼°¼ÓČČ×°ÖĆŅŃĀŌČ„![]() ”¢ÓŠ¹ŲŹż¾ŻŗĶŹµŃé²½ÖčČēĻĀĖłŹ¾”£
”¢ÓŠ¹ŲŹż¾ŻŗĶŹµŃé²½ÖčČēĻĀĖłŹ¾”£
ĪļÖŹ | Ļą¶Ō·Ö×ÓÖŹĮæ | ĆÜ¶Č | ·Šµć | ŌŚĖ®ÖŠµÄČܽāŠŌ |
ŅŅ“¼ | 46 |
| 80 | ŅŌČĪŅā±Č»„ČÜ |
ŅŅĖį | 60 |
| 118 | Ņ×ČÜ |
ŅŅĖįŅŅõ„ | 88 |
| 77 | ÄŃČÜ |
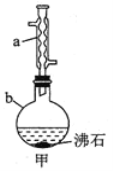
ŹµŃé²½Öč£ŗ
![]() ĻņŅĒĘ÷bÖŠ¼ÓČė9.5 mLŅŅ“¼£Ø¹żĮ棩ŗĶ6 mLŅŅĖį£¬ŌŁ»ŗĀż¼ÓČė2.5 mLÅØĮņĖį£¬»ģŗĻ¾łŌČŗ󣬼ÓČė·ŠŹÆ£¬Č»ŗó×°ÉĻĄäÄż¹Ü
ĻņŅĒĘ÷bÖŠ¼ÓČė9.5 mLŅŅ“¼£Ø¹żĮ棩ŗĶ6 mLŅŅĖį£¬ŌŁ»ŗĀż¼ÓČė2.5 mLÅØĮņĖį£¬»ģŗĻ¾łŌČŗ󣬼ÓČė·ŠŹÆ£¬Č»ŗó×°ÉĻĄäÄż¹Ü![]() ČēĶ¼¼×ĖłŹ¾
ČēĶ¼¼×ĖłŹ¾![]() ”£
ӣ
![]() Š”»š¼ÓČČŅĒĘ÷b£¬»ŗĀż»ŲĮ÷0.5 h£¬“żĘæÄŚ·“Ó¦ĪļĄäČ“ŗ󣬽«»ŲĮ÷×°ÖĆøijÉÕōĮó×°ÖĆ£¬¼ÓČČÕō³öŅŅĖįŅŅõ„”£
Š”»š¼ÓČČŅĒĘ÷b£¬»ŗĀż»ŲĮ÷0.5 h£¬“żĘæÄŚ·“Ó¦ĪļĄäČ“ŗ󣬽«»ŲĮ÷×°ÖĆøijÉÕōĮó×°ÖĆ£¬¼ÓČČÕō³öŅŅĖįŅŅõ„”£
![]() ĻņĮó³öŅŗÖŠ»ŗĀż¼ÓČė5mL±„ŗĶĢ¼ĖįÄĘČÜŅŗ£¬Õńµ“£¬Ö±ÖĮ²»ŌŁÓŠ¶žŃõ»ÆĢ¼ĘųĢå²śÉś£¬Č»ŗ󽫻ģŗĻŅŗ×ŖŅĘÖĮ·ÖŅŗĀ©¶·ÖŠ£¬·ÖČ„Ė®²ć£¬½«ÓŠ»ś²ćŅĄ“ĪÓĆ5mL±„ŗĶŹ³ŃĪĖ®ŗĶ5mL±„ŗĶĀČ»ÆøĘČÜŅŗĻ“µÓŗó£¬×ŖŅĘÖĮ׶ŠĪĘæÖŠ£¬¼ÓČėÉŁĮæĪŽĖ®
ĻņĮó³öŅŗÖŠ»ŗĀż¼ÓČė5mL±„ŗĶĢ¼ĖįÄĘČÜŅŗ£¬Õńµ“£¬Ö±ÖĮ²»ŌŁÓŠ¶žŃõ»ÆĢ¼ĘųĢå²śÉś£¬Č»ŗ󽫻ģŗĻŅŗ×ŖŅĘÖĮ·ÖŅŗĀ©¶·ÖŠ£¬·ÖČ„Ė®²ć£¬½«ÓŠ»ś²ćŅĄ“ĪÓĆ5mL±„ŗĶŹ³ŃĪĖ®ŗĶ5mL±„ŗĶĀČ»ÆøĘČÜŅŗĻ“µÓŗó£¬×ŖŅĘÖĮ׶ŠĪĘæÖŠ£¬¼ÓČėÉŁĮæĪŽĖ®![]() ¹ĢĢ壬¾²ÖĆʬæĢ£¬¹żĀĖ³żČ„
¹ĢĢ壬¾²ÖĆʬæĢ£¬¹żĀĖ³żČ„![]() ¹ĢĢå£¬Č»ŗó½«ÓŠ»ś²ć½ųŠŠÕōĮó“æ»Æ£¬ŹÕ¼Æ
¹ĢĢå£¬Č»ŗó½«ÓŠ»ś²ć½ųŠŠÕōĮó“æ»Æ£¬ŹÕ¼Æ![]() Ź±µÄĮó·Ö£¬µĆµ½
Ź±µÄĮó·Ö£¬µĆµ½![]() ŅŅĖįŅŅõ„”£
ŅŅĖįŅŅõ„”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŹµŃéŌĄķ£ŗŅŅĖįÓėŅŅ“¼ŌŚ“߻ƼĮ“ęŌŚµÄĢõ¼žĻĀ¼ÓČČæÉŅŌ·¢Éśõ„»Æ·“Ӧɜ³ÉŅŅĖįŅŅõ„£¬ĒėÓĆŃõĶ¬Ī»ĖŲŹ¾×Ł·ØŠ“³öCH3CO18OHÓėCH3CH2OH·¢Éśõ„»Æ·“Ó¦µÄ»Æѧ·½³ĢŹ½”£______________”£
£Ø2£©ŅĒĘ÷aµÄĆū³ĘĪŖ______________£¬ŅĒĘ÷bµÄ¹ęøńĪŖ_______![]() Ģī×ÖÄø
Ģī×ÖÄø![]() ”£
ӣ
A£®25 mL B£®50mL C£®250 mL D£®500mL ![]()
£Ø3£©²½Öč![]() ÖŠ£¬½«Įó³öŅŗ¾±„ŗĶĢ¼ĖįÄĘČÜŅŗ“¦ĄķŗóµÄ»ģŗĻŅŗÖĆÓŚ·ÖŅŗĀ©¶·ÖŠ£¬Õńµ“ŗó¾²ÖĆ£¬Ė®²ćŌŚ________
ÖŠ£¬½«Įó³öŅŗ¾±„ŗĶĢ¼ĖįÄĘČÜŅŗ“¦ĄķŗóµÄ»ģŗĻŅŗÖĆÓŚ·ÖŅŗĀ©¶·ÖŠ£¬Õńµ“ŗó¾²ÖĆ£¬Ė®²ćŌŚ________![]() Ģī”°ÉĻ²ć”±»ņ”°ĻĀ²ć”±
Ģī”°ÉĻ²ć”±»ņ”°ĻĀ²ć”±![]() ”£
ӣ
£Ø4£©ŌŚ²½Öč![]() ÖŠ£¬¼ÓČėÉŁĮæĪŽĖ®ĮņĖįĆ¾¹ĢĢåµÄ×÷ÓĆŹĒ__________________________”£
ÖŠ£¬¼ÓČėÉŁĮæĪŽĖ®ĮņĖįĆ¾¹ĢĢåµÄ×÷ÓĆŹĒ__________________________”£
£Ø5£©õ„²ćŗń¶ČµÄ±ź¶Ø£ŗ¼ÓČČ»ŲĮ÷Ņ»¶ĪŹ±¼äŗóŌŁÕō³ö²śĪļ£¬ĪŖĮĖøüŗƵŲ²ā¶ØÓŠ»ś²ćŗń¶Č£¬æÉŌ¤ĻČĻņ±„ŗĶĢ¼ĖįÄĘČÜŅŗÖŠ¼ÓČė1µĪ_________ŹŌŅŗ£¬ĻÖĻóŹĒ ___________________”£
£Ø6£©øĆŹµŃéÖŠŅŅĖįŅŅõ„µÄ²śĀŹĪŖ_______ (¼ĘĖć½į¹ū¾«Č·µ½![]() )”£
)ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹Ų°±µÄŠšŹöÕżČ·µÄŹĒ£Ø £©
A. æÉÓĆĻņÉĻÅÅæÕĘų·ØŹÕ¼Æ°±Ęų
B. °±Ęų¼«Ņ×ČÜÓŚĖ®£¬Ņņ“Ė¼ÓČČÅØ°±Ė®²»»į²śÉś°±Ęų
C. ½«Į½øł·Ö±šÕŗÓŠÅØ°±Ė®ŗĶÅØĮņĖįµÄ²£Į§°ōææ½üŹ±£¬ÓŠ°×ŃĢÉś³É
D. ŌŚŹµŃéŹŅÖŠ£¬æÉÓĆ¼ÓČČĒāŃõ»ÆøĘŗĶĀČ»Æļ§µÄ¹ĢĢå»ģŗĻĪļµÄ·½·ØÖĘČ”°±Ęų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĻĀĶ¼ĖłŹ¾£¬°ŃŹŌ¹Ü·ÅČėŹ¢ÓŠ25 ”걄ŗĶCa(OH)2ČÜŅŗµÄÉÕ±ÖŠ£¬ŹŌ¹ÜæŖŹ¼·ÅČė¼øŠ”æéĆ¾Ę¬£¬ŌŁÓƵĪ¹ÜµĪ5 mLŃĪĖįÓŚŹŌ¹ÜÖŠ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©ŹµŃéÖŠ¹Ū²ģµ½µÄĻÖĻóŹĒ______________________________________________________”£
£Ø2£©²śÉśÉĻŹöĻÖĻóµÄŌŅņŹĒ___________________________________”£
£Ø3£©Š“³öÓŠ¹ŲµÄĄė×Ó·½³ĢŹ½£ŗ________________________________________”£
£Ø4£©ÓÉŹµŃéĶĘÖŖ£¬MgCl2ČÜŅŗŗĶH2µÄ×ÜÄÜĮæ________(Ģī”°“óÓŚ”±”°Š”ÓŚ”±»ņ”°µČÓŚ£¬ĻĀĶ¬”±)Ć¾Ę¬ŗĶŃĪĖįµÄ×ÜÄÜĮ棬¦¤H________0”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉś²śĮņĖį¹ż³ĢÖŠ£¬SO2ŌŚ½Ó“„ŹŅÖŠ±»“ß»ÆŃõ»ÆĪŖSO3ĘųĢ壬ŅŃÖŖøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦”£ĻÖ½«2 mol SO2”¢1 mol O2³äČėŅ»ĆܱÕČŻĘ÷³ä·Ö·“Ó¦ŗ󣬷ųöČČĮæ98£®3 kJ£¬“ĖŹ±²āµĆSO2µÄ×Ŗ»ÆĀŹĪŖ50%£¬ŌņĻĀĮŠČČ»Æѧ·½³ĢŹ½ÕżČ·µÄŹĒ
A. 2SO2(g)£«O2(g)![]() 2SO3(g) ¦¤H£½£196£®6 kJ”¤mol£1
2SO3(g) ¦¤H£½£196£®6 kJ”¤mol£1
B. 2SO2(g)£«O2(g)![]() 2SO3(g) ¦¤H£½£98£®3 kJ”¤mol£1
2SO3(g) ¦¤H£½£98£®3 kJ”¤mol£1
C. SO2(g)£«![]() O2(g)
O2(g)![]() SO3(g) ¦¤H£½£«98£®3 kJ”¤mol£1
SO3(g) ¦¤H£½£«98£®3 kJ”¤mol£1
D. SO2(g)£«![]() O2(g)
O2(g)![]() SO3(g) ¦¤H£½£196£®6 kJ”¤mol£1
SO3(g) ¦¤H£½£196£®6 kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com