
【题目】有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL该溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生;(2)第二份加足最NaOH溶液加热后,收集到气体0.04 mol;(3)第三份加足量BaCl2溶液后,干燥后得到沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,下列推测正确的是
①K+一定存在;②100mL溶液中含0.01molCO32-;③Cl-可能存在;④ Ba2+一定不存在;⑤Mg2+可能存在
A. ②③④ B. ③④⑤ C. ①②③ D. ①③④
【答案】D
【解析】第一份:第一份加入AgNO3,溶液有沉淀产生,说明溶液中可能存在:Cl-、CO32-、SO42-;第二份:加足量NaOH溶液加热后生成标准状况下0.896L气体为氨气,则溶液中一定含有NH4+,且物质的量为![]() =0.04mol;第三份:根据题中信息可知2.33为硫酸钡,n(BaSO4)=n(SO42-)=
=0.04mol;第三份:根据题中信息可知2.33为硫酸钡,n(BaSO4)=n(SO42-)=![]() =0.01mol;6.27g为硫酸钡和碳酸钡,所以碳酸钡的物质的量为:
=0.01mol;6.27g为硫酸钡和碳酸钡,所以碳酸钡的物质的量为: ![]() =0.02mol;因为一定含CO32-所以不含Mg2+;再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.04mol;n(-)=2n(CO32-)+2n(SO42-)=0.06mol,故一定有K+,至少0.02mol;①K+一定存在,故正确;②100mL溶液中含0.02molCO32-,故错误;③因含有CO32-、SO42-,故实验过程中无法对Cl-的检验进行确定,无法确定是否含有Cl-,Cl-可能存在,故正确;④ Ba2+一定不存在,故正确;⑤Mg2+一定不存在,故错误。答案选D。
=0.02mol;因为一定含CO32-所以不含Mg2+;再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.04mol;n(-)=2n(CO32-)+2n(SO42-)=0.06mol,故一定有K+,至少0.02mol;①K+一定存在,故正确;②100mL溶液中含0.02molCO32-,故错误;③因含有CO32-、SO42-,故实验过程中无法对Cl-的检验进行确定,无法确定是否含有Cl-,Cl-可能存在,故正确;④ Ba2+一定不存在,故正确;⑤Mg2+一定不存在,故错误。答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】现通过以下步骤由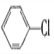 制备
制备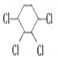
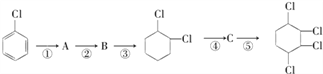
(1)写出A、B的结构简式:A_________, B________。
(2)从左到右依次填写每步反应所属的反应类型____________(a.取代反应;b.加成反应;c.消去反应。只填字母代号)。
(3)写出反应A→B所需的试剂和条件:_____________。
(4)写出④和⑤的化学方程式___________________,________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推断正确的是
A. pH=6.5的溶液一定显酸性
B. 0.1mol L-1的Na2CO3溶液中:c(CO32-)+c(HCO3-)=0.1mol L-1
C. 常温下,等体积的0.2 mol L-1的盐酸与0.2 mol L-1的氢氧化钡溶液混合,所得溶液的pH=13
D. 常温下,某溶液中水电离出的c(OH-)=l×10-12 mol L-1,该溶液pH 一定等于2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是课外活动小组设计的用化学电源使LED灯发光装置.下列说法不正确的是( ) 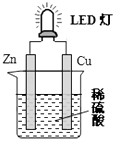
A.锌是负极,电子从锌片经导线流向铜片
B.氢离子在铜片表面被还原
C.装置中存在“化学能→电能→光能”的转换
D.如果将硫酸换成橙汁,导线中不会有电子流动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物的叙述,正确的是
A.淀粉、纤维素和油脂都属于天然高分子化合物
B.糖类、植物油和蚕丝在一定条件下都能够发生水解反应
C.石油的分馏所得的馏分一定都是纯净物
D.苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋是一种绿色稀有金属,铋及其化合物在工业生产中用途广泛,工业上常采用粗铋精炼制得用途更为广泛的精炼铋(含铋99.995%),火法精炼铋的工艺流程如下:

已知:①粗铋(铅铋合金)的主要化学成分如下表:
元素 | Ag | Bi | Pb | As | Sb |
含量/% | 0.90 | 55.25 | 27 | 1.30 | 11 |
②氯化铅熔点为498℃,密度为5.9g/cm3;铋的熔点为271℃,沸点为1470℃;BiCl3的熔点为506.5℃。
③锌酸盐简写成ZnO22-,如锌酸钠Na2ZnO2。
④+3价铋的化合物较为稳定,铋酸钠难溶于水。
回答下列问题:
(1)实验室中升温熔化粗铋一般用酒精喷灯在________(填主要仪器名称)中完成。
(2)NaBiO3中铋元素的化合价为________。
(3)“氧化除砷锑”的工艺机理是粗铋熔融液在680~750℃的条件下,鼓入压缩空气,使砷、锑氧化挥发,同时空气也与铋液反应,利用Bi2O3的_______性将杂质砷、锑转变成As2O3、Sb2O3而除去。
(4)“氯化除铅”过程中,氯气与铅、铋反应分别生成PbCl2、BiCl3,生成的BiCl3又会被铅还原,发生反应3Pb+2BiCl3=3PbC12+2Bi,控制温度350-400℃,利用熔点和密度特点,氯化铅上浮至铋液表面呈_______态覆盖,防止氯气__________________。
(5)高温精炼的实质为碱性精炼,加入少量KNO3和NaOH,将锌氧化成锌酸盐而除去残锌,同时得到氮气,写出高温精炼的化学方程式: __________________。
(6)向含有MnSO4的酸性溶液中加入铋酸钠粉末,溶液变为紫红色,该反应经常用来检验Mn2+,写出该反应的离子方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.反应A: 4HCl+O2 ![]() 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4mol HCl被氧化,放出115.6kJ的热量.
ⅱ. 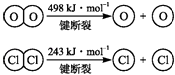
(1)反应A的热化学方程式是 .
(2)断开1mol H﹣O键与断开1mol H﹣Cl键所需能量相差约为kJ,H2O中H﹣O键比HCl中H﹣Cl键(填“强”或“弱”) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z都是金属,把X放入Z的盐溶液中,X的表面附着一层Z;X与Y组成原电池时,X为电池的正极。X、Y、Z三种金属的活动性顺序是
A. X>Y>Z B. X>Z>Y C. Y>X>Z D. Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A. 常温下,pH=3的盐酸与pH=11的氨水溶液中水的电离程度相同
B. 常温下两种溶液①0.1mol/L CH3COOH溶液 ②0.3mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积的混合液,c(H+):①>②
C. 室温下向10mL pH=3的醋酸溶液中加入水稀释后溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]不变
D. MOH和ROH两种碱的溶液分别加水稀释时,pH变化如图所示则稀释前,c(ROH)<10c(MOH)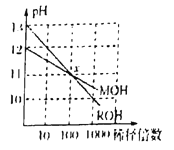
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com