
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应:Mn2++S2O +H2O→MnO
+H2O→MnO +SO
+SO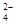 +H+,下列说法不正确的是(
)
+H+,下列说法不正确的是(
)
A.可以利用该反应检验Mn2+
B.配平后的系数为2、5、8、2、10、16
C.该反应中酸性介质不能为盐酸
D.若有0.1mol还原产物生成, 则转移电子0.5mol
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
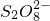 +H2O→MnO4-+
+H2O→MnO4-+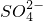 +H+,下列说法不正确的是
+H+,下列说法不正确的是查看答案和解析>>
科目:高中化学 来源:2013届安徽省阜阳一中高三第一次月考化学试卷(带解析) 题型:单选题
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应:Mn2++S2O +H2O→MnO
+H2O→MnO +SO
+SO +H+,下列说法不正确的是( )
+H+,下列说法不正确的是( )
| A.可以利用该反应检验Mn2+ |
| B.配平后的系数为2、5、8、2、10、16 |
| C.该反应中酸性介质不能为盐酸 |
| D.若有0.1mol还原产物生成, 则转移电子0.5mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com