
相对分子质量为100的有机物A能与钠反应,且完全燃烧只生成CO2和H2O。若A含一个六碳环,则环上一氯代物的数目为(不考虑空间异构)
A.5 B.4 C.3 D.2
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源:2015-2016学年山东省滕州市高一上学期12月月考化学试卷(解析版) 题型:选择题
一定能在下列溶液中大量共存的离子组是
A.1.0mol/L的KNO3溶液:H+、Fe2+、Cl -、SO42-
-、SO42-
B.强碱性溶液:Na+、HCO3-、NO3-、SO42-
C.遇酚酞变红的溶液中:K+、Na+ 、NH4+、Br-
、NH4+、Br-
D.强酸性溶液:Na+、NH4+、SO42-、Cl-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省平度市高二上学期直升班抽考化学试卷(解析版) 题型:选择题
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的①NaOH固体 ②H2O ③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A.②④⑥ B.①② C.②③⑤ D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高二上诊断检测化学试卷(解析版) 题型:填空题
(1)某温度时,水的离子积Kw=1×10-13,则该温度_________25℃(填“>”、“<”或“=”)。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10 mol•L-1,则该溶液的pH可能为________;
(2)若温度为25℃时,体积为Va、pH=a的H2SO4与体积为Vb、pH=b的NaOH混合,恰好中和,此溶液中各种离子的浓度由大到小的排列顺序是_____________。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上12月月考化学试卷(解析版) 题型:选择题
在密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g)
N2O4(g) 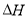 =-57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
=-57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
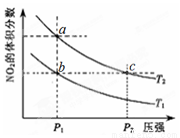
A.a、c两点的反应速率:a>c
B.a、b两点NO2的转化率:a<b
C.a、c两点气体的颜色:a深,c浅
D.由a点到b点,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上学期第五次模拟理综化学试卷(解析版) 题型:填空题
铁及其化合物在工农业生产、环境保护等领域中有着重要的作用。
(1)酸性条件下,硫酸亚铁可将MnO2还原为MnSO4,该反应的离子方程式为:_____________。
(2)分析表明,铁在浓硫酸中发生钝化时,生成的氧化物中Fe、O两种元素的质量比为28∶11,则其化学式为______________。
(3)铁及其化合物可用于消除环境污染。常温下,硫酸亚铁能将SO2转化为SO42-,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为____________________。
常温下,用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2反应可生成0.5 mol N2,则y=____________。
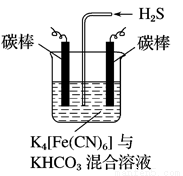
(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2CO32-+H2S=2[Fe(CN)6]4-+2HCO3-+S↓。电解时,阳极的电极反应式为___________;电解过程中阴极区溶液的pH______________(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期12月月考化学试卷(解析版) 题型:选择题
有机物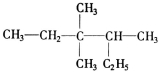 的正确命名为
的正确命名为
A.2-乙基-3,3-二甲基-4-乙基戊烷
B.3,3-二甲基-4-乙基戊烷
C.3,3,4-三甲基已烷
D.2,3,3-三甲基已烷
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列物质中既属于芳香化合物又属于醇的是( )
A.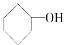 B.
B.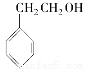
C.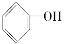 D.CH3CH2OH
D.CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上学期12月月考化学试卷(教师版) 题型:选择题
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内是离子“流过”水和氧化锌组成的电解液。电池总反应为:
Zn + 2 MnO2十H2O = ZnO + 2MnO(OH)。下列说法正确的是
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.当 0.lmol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023
D.电池正极反应式为: 2MnO2 + 2e一+ 2H2O = 2MnO (OH)十2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com