
| A. | 放电时Cl-由负极向正极迁移 | |
| B. | 正极反应式为:AgCl+e-=Ag+Cl- | |
| C. | Mg作电池负极,发生氧化反应 | |
| D. | 当负极质量减轻4.8g,电路中通过0.4mol电子 |
分析 Mg-AgCl电池中,活泼金属Mg是还原剂、AgCl是氧化剂,所以金属Mg作负极,反应式为:Mg-2e-=Mg2+,正极反应为:2AgCl+2e-═2C1-+2Ag,阴离子移向负极,据此分析.
解答 解:A.原电池放电时,阴离子向负极移动,则Cl-在正极产生由正极向负极迁移,故A错误;
B.AgCl是难溶物,正极反应式为:AgCl+e-═C1-+Ag,故B正确;
C.活泼金属镁作负极,失电子发生氧化反应,故C正确;
D.活泼金属镁作负极,反应式为:Mg-2e-=Mg2+,则当负极质量减轻4.8g,电路中通过$\frac{4.8g}{24g/mol}$×2=0.4mol电子,故D正确;
故选:A.
点评 本题考查原电池工作原理,注意常见物质的性质,如镁的还原性以及银离子的氧化性是解题的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:W>X>Y>Z | |
| B. | 简单氢化物的稳定性:W<X | |
| C. | 最高价氧化物对应水化合物的碱性:Y>Z | |
| D. | Y的单质可以将Z从可溶性盐溶液中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示,将 4molSO2和2molO2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态 A 时,测得气体总物质的量为 4.2mol.若SO2、O2、SO3的起始物质的量分别用 a、b、c表示,回答下列问题:
如图所示,将 4molSO2和2molO2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态 A 时,测得气体总物质的量为 4.2mol.若SO2、O2、SO3的起始物质的量分别用 a、b、c表示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应必伴随能量变化 | |
| B. | 反应是放热还是吸热取决于反应物和生成物具有的总能量的相对大小 | |
| C. | 可燃物燃烧和酸碱中和反应都是典型的放热反应 | |
| D. | 燃煤发电不需经过其它能量转换过程,可直接把化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | CH4O | C. | C2H4O | D. | C2H6O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | (1)(3) | B. | (2)(4) | C. | (4) | D. | (4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 毛织、丝织衣服不宜用加酶洗衣粉洗涤 | |
| B. | 纤维素、淀粉、油脂均为天然高分子化合物 | |
| C. | 由煤的干馏可知煤中含甲苯、二甲苯、苯酚等芳香族化合物 | |
| D. | 向蛋白质溶液中滴入CuSO4溶液,蛋白质聚沉后还能溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
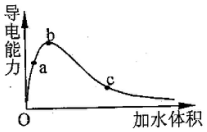
| A. | a,b,c三点溶液的pH:a>b>c | |
| B. | 若用湿润的pH试纸测试c处溶液的pH,比实际的pH偏小 | |
| C. | a,b,c三点溶液用1mol•L-1的NaOH溶液中和,消耗NaOH溶液的体积a>b>c | |
| D. | a,b,c点醋酸的电离程度:c>b>a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应达到平衡状态时A的转化率为60% | |
| B. | x=4 | |
| C. | 反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为6:5 | |
| D. | 若混合气体的密度不再变化,则该可逆反应达到化学平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com