
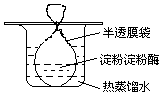
 把一定量的淀粉和少量淀粉酶配成溶胶灌于半透膜袋中并置于盛有热的蒸馏水的烧杯中(如图所示).一段时间后进行如下实验,回答相关问题.
把一定量的淀粉和少量淀粉酶配成溶胶灌于半透膜袋中并置于盛有热的蒸馏水的烧杯中(如图所示).一段时间后进行如下实验,回答相关问题.分析 (1)淀粉在淀粉酶的作用下发生水解生成葡萄糖;
(2)淀粉在淀粉酶的作用下发生水解生成葡萄糖,葡萄糖含有醛基,遇新制Cu(OH)2悬浊液中加热煮沸会生成砖红色的氧化亚铜沉淀;
(3)根据淀粉与碘水变蓝检验判断.
解答 解:(1)淀粉在淀粉酶的作用下发生水解生成葡萄糖,方程式为:(C6H10O5)n+nH2O$\stackrel{酶}{→}$nC6H12O6 ,故答案为:(C6H10O5)n+nH2O$\stackrel{酶}{→}$nC6H12O6 ;
(2)淀粉在淀粉酶的作用下发生水解生成葡萄糖,葡萄糖含有醛基,遇新制Cu(OH)2悬浊液中加热煮沸会生成砖红色的氧化亚铜沉淀,所以观察到的现象是有砖红色沉淀生成,故答案为:有砖红色沉淀生成;
(3)证明半透膜袋中的液体中含淀粉,实验方法为取半透膜袋中的液体少量滴加碘水,溶液变蓝,
故答案为:碘水;变蓝.
点评 本题考查物质的检验和鉴别,为高考常见题型,侧重于元素化合物知识及实验结合的应用,注意把握相关物质的性质及常见离子的检验方法,题目难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
| 序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 13 |
| ② | 22.00 | 18.00 | 12 |
| ③ | 22.00 | 22.00 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5:3 | B. | 5:4 | C. | 1:1 | D. | 4:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于2HI(g)?H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 | |
| B. | 溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 | |
| C. | 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 | |
| D. | 反应CO(g)+NO2(g)?CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
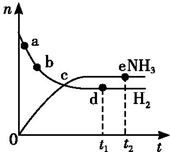 向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示.下列有关叙述一定正确的是( )
向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示.下列有关叙述一定正确的是( )| A. | c点表示NH3生成速率与NH3分解速率相等 | |
| B. | c点和e点H2的转化率相等 | |
| C. | 平衡后再升高温度,不利于氨的合成 | |
| D. | d点时:n(H2):n(NH3)=3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com