
【题目】氯胺(NH2Cl,Cl的化合价为+1价)是一种长效缓释有机氯消毒剂,它与水可以发生复分解反应。有关氯胺的说法错误的是
A.氯胺中的氮元素为-3价
B.氯胺与水反应的产物为NH2OH和HCl
C.氯胺的消毒原理与漂粉精相似
D.氯胺的消毒效率(单位质量的消毒剂得到的电子数)是Cl2的1.38倍
【答案】B
【解析】
A.由题可知氯胺中Cl的化合价为+1,经过计算N的化合价为-3,A项正确;
B.由题可知,氯胺和水发生的是复分解反应,复分解反应是非氧化还原反应,不涉及元素变价,因此产物应为NH3和HClO,B项错误;
C.氯胺与水反应会生成HClO,HClO具有强氧化性可杀菌消毒;漂粉精中的有效成分Ca(ClO)2由于具有强氧化性,可用于杀菌消毒,因此二者消毒原理相似,C项正确;
D.氯胺中的Cl是+1价,1个氯胺可以得2个电子,因此单位质量的氯胺得电子的物质的量为:![]() mol;1个Cl2可以得2个电子,因此单位质量的氯气得电子的物质的量为:
mol;1个Cl2可以得2个电子,因此单位质量的氯气得电子的物质的量为:![]() ,所以氯胺的消毒效率是氯气的
,所以氯胺的消毒效率是氯气的![]() 倍,D项正确;
倍,D项正确;
答案选B。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)运动员服用兴奋剂的现象在世界大赛中时有发生,某种兴奋剂的结构如图。回答下列问题。
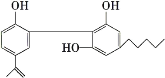
①它的化学式为____。
②从结构上看,它属于___类。
③它所含的官能团的名称是___。
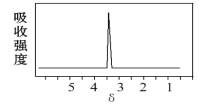
(2)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图:则A的名称为___;请预测B的核磁共振氢谱上有___个峰(信号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.分别只用一种试剂除去下列各组中所含的少量杂质(括号内为杂质),在空格中填上需加入最适合的一种试剂:
(1)FeCl3溶液(FeCl2)________________,
(2)FeCl2溶液(FeCl3)________________,
(3)Fe 粉末(Al) _______________,
Ⅱ.为测定某镁铝合金样品中铝的含量,进行了下列实验:取一定量合金,加入100 mL 0.3 mol·L-1稀硝酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去300 mL NaOH溶液。则所取样品中铝的物质的量为___________,反应中转移的电子数为______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显血红色,它们相互转化关系如图所示。
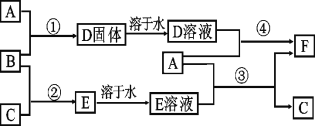
请回答:
(1)写出B物质的化学式:_______;F的化学名称:_______。
(2)写出第②步C在B中燃烧的反应现象:_______。
(3)写出第④步反应的化学反应方程式_______。
(4)F溶液中滴入NaOH溶液可能产生的实验现象是____,写出该反应的化学方程式_____________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若将0.2 mol钠、镁、铝分别投入到10 mL 1 mol·L-1盐酸中,在标准状况下产生氢气的体积由大到小的顺序是
A.V(Na)=V(Al)=V(Mg)B.V(Al)>V(Mg)>V(Na)
C.V(Al)=V(Mg)>V(Na)D.V(Na)>V(Al)=V(Mg)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对烟道气中的SO2进行吸收或回收再利用具有一定的社会和经济价值。
请回答下列问题:
(1)用NaOH溶液吸收SO2 ,写出相关反应的离子方程式_______________________。
(2)已知NaHSO3溶液显酸性,比较NaHSO3溶液中c(H2SO3)_____ c(SO32-)(填“>”“<”或“=”),请简述判断理由____________________________________________。
烟道气中的SO2,也可通过如下反应回收硫:2CO(g)+SO2(g)![]() S(s)+2CO2(g) + Q kJ。某温度下,在2 L恒容密闭容器中通入2 mol SO2和一定量的CO,发生上述反应,5 min后达到平衡,生成1 mol CO2。
S(s)+2CO2(g) + Q kJ。某温度下,在2 L恒容密闭容器中通入2 mol SO2和一定量的CO,发生上述反应,5 min后达到平衡,生成1 mol CO2。
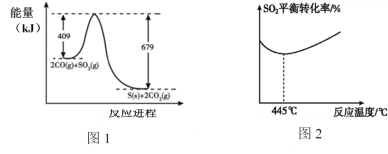
(3)一定条件下,上述反应的能量变化如图1,则 Q =_________kJ。
(4)写出该反应平衡常数表达式________;0~5min内SO2的平均反应速率为________。
(5)对反应2CO(g)+SO2(g)![]() S(s)+2CO2(g) + Q kJ的分析正确的是_______。
S(s)+2CO2(g) + Q kJ的分析正确的是_______。
a.若混合气体密度保持不变,则反应已达平衡状态
b.从反应开始到平衡时,容器内气体的压强保持不变
c.平衡时,其它条件不变,分离出硫,正反应速率加快
d.平衡时,其它条件不变,再充入一定量CO2,平衡常数保持不变
(6)其他条件不变时,随着温度的升高,SO2的平衡转化率随温度的变化曲线如图2所示,请解释其可能的原因________________________________。(已知硫的沸点约是445°C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液中的离子平衡是中学学习的一个重要内容。请回答下列有关问题。
(1)常温下,用0.1000mol/L氨水滴定盐酸,当达到滴定终点时,溶液pH___7(填“>”、“<”或“=”),为了减小滴定误差,在滴定实验中使用的酸碱指示剂最好是___。(填字母)
A、甲基橙 B、酚酞 C、石蕊 D、以上均可
(2)常温下,将1 mL pH=12的NaOH溶液加水稀释到100mL,稀释后溶液中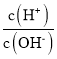 =___。
=___。
(3)某温度下,测得0.1 mol/LNaOH溶液pH为11,则该温度下水的离子积常数Kw=___。
(4)浓度相等的盐酸和醋酸各100mL,分别与过量的Zn反应,相同条件下生成H2的体积分别为V1和V2,则V1____V2(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“类推思维”是化学解题中常用的思维方法,类推的结论最终要经过实践的检验,才能决定其正确与否。下列类推结论中正确的是
A.钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
B.铝在空气中生成氧化膜保护内层金属;铁在空气中生成氧化膜也保护内层金属
C.Al(OH)3、Cu(OH)2受热易分解;Fe(OH)3受热也易分解
D.Fe与CuSO4溶液反应能置换Cu;Na与CuSO4溶液反应也能置换Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A. 使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl-
B. ![]() =1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
=1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
C. 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42-
D. 水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、AlO2-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com