
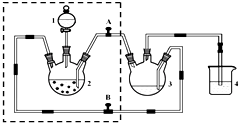
 Na2S2O4是重要的工业漂白剂,某化学小组欲制备Na2S2O4(如图)并探究其性质.现将1.5mol/L的HCOONa溶液和0.5mol/L NaOH溶液等体积注入三颈烧瓶,发生反应:HCOONa+2SO2+NaOH═Na2S2O4+CO2+H2O
Na2S2O4是重要的工业漂白剂,某化学小组欲制备Na2S2O4(如图)并探究其性质.现将1.5mol/L的HCOONa溶液和0.5mol/L NaOH溶液等体积注入三颈烧瓶,发生反应:HCOONa+2SO2+NaOH═Na2S2O4+CO2+H2O| 实验步骤 | 现象及结论 |
| 步骤Ⅰ:对三颈烧瓶分离出的产品进行重结晶得到纯净的Na2S2O4(仅需说明方法) | |
| 步骤Ⅱ:取0.1g步骤Ⅰ的产品溶于5mL银氨溶液,振荡,水浴加热10s,观察现象 | 若10S出现银镜,则甲的结论正确(或Na2S2O4具有还原性),反之则乙正确 |
分析 a中70%的浓硫酸通过分液漏斗滴到蒸馏烧瓶中和亚硫酸钠反应:Na2SO3+H2SO4(浓)═Na2SO4+H2O+SO2↑,制得二氧化硫,二氧化硫和NaOH和HCOONa在三颈烧瓶中进行反应,HCOONa+2SO2+NaOH═NaS2O4+CO2+H2O,装置C为氢氧化钠吸收尾气,防止二氧化硫污染空气.
(l)分液漏斗有活塞,能控制滴加液体的速率;c装置吸收尾气,防止二氧化硫污染空气;
(2)浓硫酸与亚硫酸钠反应生成硫酸钠、水和二氧化硫,分液漏斗有活塞,通过分液漏斗颈部活塞控制低价硫酸的快慢,控制b中反应速率;
(3)HCOONa结构中含有醛基(-CHO)能发生银镜反应;丙同学设计实验方案,首先需制备纯净的Na2S2O4,所以进行重结晶得到纯净的Na2S2O4,然后再进行银镜反应,排除HCOONa的干扰.
解答 解:(l)a装置有玻璃活塞,为分液漏斗,该反应中有二氧化硫污染性气体产生,防止污染空气需尾气处理装置,c装置吸收尾气,防止二氧化硫污染空气,
故答案为:分液漏斗;吸收二氧化硫,防止污染空气;
(2)浓硫酸与亚硫酸钠的反应的化学方程式为:Na2SO3+H2SO4(浓)═Na2SO4+H2O+SO2↑,分液漏斗有玻璃活塞,可通过旋转玻璃活塞控制滴加液体反应物的速率实现控制b中反应速率,
故答案为:Na2SO3+H2SO4(浓)═Na2SO4+H2O+SO2↑;通过分液漏斗颈部活塞控制低价硫酸的快慢;
(3)HCOONa结构中含有醛基(-CHO)能发生银镜反应,乙同学认为上述实验不能说甲的结论一定成立,可能是HCOONa过量,分离出的晶体所含杂质HCOONa具有还原性也能发生银镜反应,针对甲、乙同学的分歧,丙同学为了验证Na2S2O4银氨溶液反应形成银镜,首先需制备纯净的Na2S2O4,所以对三颈烧瓶分离出的产品进行重结晶得到纯净的Na2S2O4,
银镜反应需碱性过量,所以取0.1g步骤Ⅰ的产品溶于5mL银氨溶液,振荡,水浴加热10s,观察现象,若10S出现银镜,则甲的结论正确(或Na2S2O4具有还原性),反之则乙正确
故答案为:因为HCOONa过量,分离出的晶体所含杂质HCOONa具有还原性也能发生银镜反应;对三颈烧瓶分离出的产品进行重结晶得到纯净的Na2S2O4;5;若10S出现银镜,则甲的结论正确(或Na2S2O4具有还原性),反之则乙正确.
点评 本题通过Na2S2O4的制备,考查物质性质实验方案的设计方法,题目难度中等,试题充分考查了学生的分析、理解能力及化学实验、化学计算能力,是一道质量较好的试题,注意甲酸钠具有还原性,能发生银镜反应.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯化铝与足量的氢氧化钠溶液反应:Al3++4OH-═AlO2-+2H2O | |
| B. | 盐酸与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| D. | 碳酸钙与硝酸反应:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④属于氧化还原反应 | B. | ①②③属于化合反应 | ||
| C. | ①②③④③③六个反应中没有分解反应 | D. | ③③属于复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:
醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题


| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用足量饱和碳酸钠溶液水洗后分液 | B. | 用足量氢氧化钠溶液水洗后分液 | ||
| C. | 加入适量乙醇和浓硫酸加热 | D. | 加入金属钠充分反应后过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com