
工业上利用氨催化氧化后,经过一系列反应可以制备硝酸。
 (1)氨气催化氧化的化学方程式为
(1)氨气催化氧化的化学方程式为
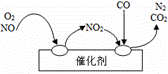
(2)给汽车安装尾气净化装置。净化装置里装有催化
剂,气体在催化剂表面吸附与解吸作用的机理如右
 图所示。写出净化过程中的总化学反应方程
图所示。写出净化过程中的总化学反应方程
式: 。
(3)目前,科学家正在研究一种以乙烯作为还原剂的
脱硝(NO)原理,其脱硝机理示意图如下图。写
出该脱硝原理总反应的化学方程式:
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
下列过程与加成反应有关的是 ( )
A.苯与溴 水混合振荡,水层颜色变浅
水混合振荡,水层颜色变浅
B.乙烯与溴水混合振荡,水层颜色变浅
C.乙烯与高锰酸钾溶液混合振荡,溶液颜色变浅
D.甲烷与氯气混合光照,气体颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
(NH4)2SO4在一定条件下发生如下反应:4(NH4)2SO4 =N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,将反应后的混合气体通入Ba(NO3)2溶液,产生的沉淀为
A.BaSO4和BaSO3 B.BaSO4 C.BaSO3 D.BaS
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各种物质在一定条件下反应,所得产物种类与反应物的用量或条件无关的是
①Fe + O2 ②Na2SiO3+CO2+ H2O ③NH4HCO3+NaOH
④Cu +Cl2 ⑤Ca(HCO3)2+Ca(OH)2 ⑥C+SiO2
A. ①②⑤ B.②③ C. ①⑤⑥ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
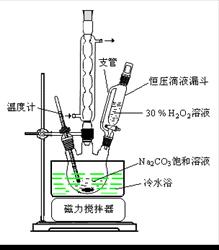
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
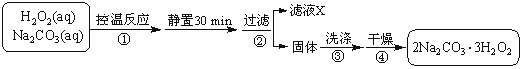
已知:主反应 2Na2CO3 (aq) + 3H2O2 (aq)  2Na2CO3·3H2O2 (s) ΔH < 0
2Na2CO3·3H2O2 (s) ΔH < 0
 副反应 2H2O2 = 2H2O + O2↑
副反应 2H2O2 = 2H2O + O2↑
50 °C时 2Na2CO3·3H2O2 (s) 开始分解
请回答下列问题:
(1)步骤①的关键是控制温度,其措施有
和 。
(2)在滤液X中加入适量NaCl固体可析出过碳酸钠,
原因是 。
(3)步骤③中选用无水乙醇洗涤产品的目的是 。
(4)下列物质中,会引起过碳酸钠失效的有 。
A.Na2S B.CuO C.Na2SiO3 D.NaHCO3
(5)过碳酸钠产品中往往含有少量碳酸钠,可用重量法测定过碳酸钠的质量分数;其操作步骤:取样品溶解→加入BaCl2溶液→ 过滤过滤
→ 洗涤洗涤
→ 干燥干燥
→ 称量。需要直接测定的物理量有: 样品的质量m1g、沉淀的质量m2g
(用字母表示并注明其含义).产品中过碳酸钠质量分数的表达式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某结晶水合物的化学式为R•nH2O,其式量为M.25℃时,将ag该晶体溶于bg水中可形成VmL饱和溶液.下列关系中正确的是( )
|
| A. | 饱和溶液的物质的量浓度为c= |
|
| B. | 25℃时R的溶解度为S= |
|
| C. | 饱和溶液中溶质的质量分数为W= |
|
| D. | 饱和溶液的密度为ρ= |
查看答案和解析>>
科目:高中化学 来源: 题型:
MnO2是中学化学中常见的一种试剂,可作氧化剂和催化剂。某兴趣小组通过实验对MnO2
的性质进行了一系列的研究。
(1)欲探究MnO2的催化效果,需要用30%的H2O2溶液(密度近似为1 g·cm-3)配制浓度为3%的H2O2溶液(密度近似为1 g·cm-3)100 mL。简述其配制方法:______________________________。
(2)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是__________。
A.把MnO2固体加入到FeS O4溶液中,再加入KSCN溶液,观察溶液是否变血红
O4溶液中,再加入KSCN溶液,观察溶液是否变血红
B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变血红
C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2溶液,观察是否有白色沉淀生成
D.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(3)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298 K,设计如下对比实验:
| 实验 | 酸或碱 | 现象 |
| A | 1滴0.2 mol·L-1 NaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1 mol·L-1硫酸 | 迅速变棕褐色 |
从上述对比实验中,可以得出的结论是_____________________________________。
写出在酸性条件下,MnO2氧化I-的离子方程式________________________________。
(4)利用二氧化锰的氧化性,让其与浓盐酸反应制取氯气,下列仪器可作为该反应的反应容器的是__________(填序号)。
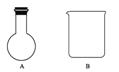
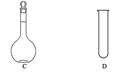
查看答案和解析>>
科目:高中化学 来源: 题型:
香叶醇是合成玫瑰香油的主要原料,其结构简式如下:
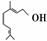 ,下列有关香叶醇的叙述正确的是 ( )
,下列有关香叶醇的叙述正确的是 ( )
A.香叶醇的分子式为C10H18O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应不能发生取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com