
某物质可能有甲醇、甲酸、乙醛、甲酸乙酯几种物质中的一种或几种,在鉴定时有下列现象:①有银镜反应,②加入新制Cu(OH)2悬浊液,沉淀不溶解,③与含有酚酞的NaOH溶液共热时发现溶液中红色逐渐变浅至无色。下列叙述中正确的是( )
| A.有甲酸乙酯和甲酸 | B.有甲酸乙酯和乙醛 |
| C.有甲酸乙酯,可能有甲醇、乙醛 | D.几种物质都有 |
科目:高中化学 来源: 题型:阅读理解
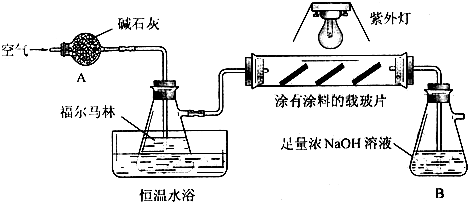
| 催化剂 |
| 紫外光 |
| 催化剂 |
| 紫外光 |
| 甲同学选择的试剂 | 乙同学认为不合理的理由 |
| 紫色石蕊试液 | 紫色石蕊试液B中溶液呈碱性(NaOH足量),无法证明是甲酸(酸性) 紫色石蕊试液B中溶液呈碱性(NaOH足量),无法证明是甲酸(酸性) |
| 新制氢氧化铜 | B中可能溶有过量的甲醛,无法证明是甲酸中醛基 B中可能溶有过量的甲醛,无法证明是甲酸中醛基 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铁是日常生活中最常见的金屑之一.某班同学在学习铁的知识时,有下列问题:
铁是日常生活中最常见的金屑之一.某班同学在学习铁的知识时,有下列问题:查看答案和解析>>
科目:高中化学 来源:内江二模 题型:问答题
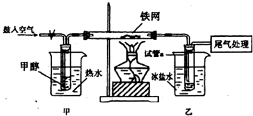
查看答案和解析>>
科目:高中化学 来源:内江二模 题型:问答题
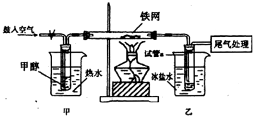
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com